Разряд - катион
Cтраница 2
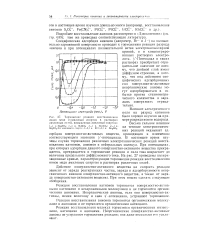 |
Торможение реакции восстановления ионов меди я-амиловым спиртом в растворах различных солей, насыщенных амиловым спиртом. [16] |
Влияние электрического поля на разряд катионов было хорошо изучено на примере разряда ионов водорода. [17]
 |
Реакция взаимодействия воды с амальгамой натрия. [18] |
В большинстве же случаев разряд катионов электроотрицательных ме-тйллов возможен в интервале рН от 0 до 5, что соответствует обратимым потенциалам разряда ионов водорода от 0 до - 0 25 в. [19]
Наиболее полное элиминирование процесса разряда катионов водорода достигается в эфирно-гидридных электролитах. Электровыделение алюминия из эфирно-гидридных электролитов часто сопровождается выделением ( хотя и незначительным) водорода, не имеющим связи с электродным процессом. [20]
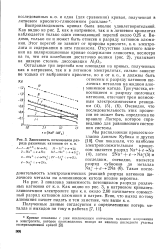 |
Зависимость потенциалов разряда различных катионов от к. о. [21] |
Такая последовательность электрохимических реакций разряда катионов щелочного металла на алюминиевом катоде вполне вероятна. [22]
Установление природы поляризации при разряде катионов одного сорта производится анализом экспериментальных поляризационных кривых. Один из таких методов анализа сводится к установлению подчинения экспериментальных данных уравнениям зависимости ( 8) - ( 11) между скоростью процесса и потенциалом электрода или перенапряжением выделения металла на катоде. [23]
В дальнейшем на катоде происходит разряд катионов притекающими к нему электронами с образованием нейтральных атомов. В результате этого происходит разрушение анодной зоны, ц чем активнее электролит ( больше концентрация солей, кислот, щелочей), тем интенсивнее анодное разрушение металла. [24]
Катодной лимитирующей реакцией может быть разряд катиона, а анодной - отрыв электрона от пиридина, с вероятным образованием иона ( пиридил-2) пириднния. [25]
Гейровский, также наблюдавший торможение разряда катионов РЬ2 и Zn2 в присутствии больших количеств пиридина, высокомолекулярных жирных кислот и спиртов [318], объяснил его иначе. [26]
В системе координат г-ср деполяризация разряда катиона металла при образовании сплава обнаруживается сдвигом парциальной поляризационной кривой разряда катиона в сторону положительных значений потенциалов относительно положения поляризационной кривой, соответствующей процессу выделения одного металла на катоде. При сверхполяризации сдвиг парциальной поляризационной кривой происходит в отрицательную сторону. [27]
О возможности использования эффекта деполяризации разряда катионов электроотрицательного компонента для получения сплавов в литературе имеются неоднократные упоминания. [28]
На первой стадии восстановления (3.1) происходит разряд катиона с потерей им гидратной оболочки и адсорбция на поверхности электрода. Вторая стадия (3.2) заключается в образовании молекул водорода путем рекомбинации ионов Щадс. [29]
В стадии ( в) совмещены разряд катиона и взаимодействие полученного атома с уже имеющимся на электроде атомом, находящимся в адсорбированном состоянии. По-видимому, процесс ( в) в отдельных случаях имеет существенное значение. [30]
Страницы: 1 2 3 4