Барьерный разряд
Cтраница 1
Барьерный разряд возбуждается в узкой полости между двумя электродами. Для ограничения плотности тока и равномерного распределения разряда вдоль электродов в рабочую зону разряда вводится диэлектрик, которым при достаточной толщине может стать и сам обрабатываемый материал. [1]
В барьерном разряде происходят разрушения молекул на радикалы и атомы и последующие вторичные реакции. Например, из газообразных углеводородов образуются различные жидкие и твердые углеводороды. Конструкции высокочастотных промышленных трубчатых озонаторов разработаны в МГУ им. [2]
Так как мощность барьерного разряда пропорциональна частоте питающего тока и при 50 периодах очень мала, в данной установке питание осуществлялось переменным током частотой 500 периодов / сек. [4]
Для реакций окисления углеводородов в барьерном разряде характерно образование продуктов неполного окисления, главным образом различных перекисей. Так, при ( Пропускании 584 л смеси метана с кислородом ( 64 % СН4, 35 % О2) через барьерный разряд было получено около 940 г жидкости, содержащей до 9 % активного кислорода. В продуктах фракционированной перегонки этой жидкости обнаружены метилформиат, метиловый спирт, муравьиная кислота, формальдегид и вода. [5]
Из возможных методов получения озона используют барьерный разряд, электролиз, фотохимический способ и высокочастотное электрическое поле. В практической деятельности наиболее часто синтез озона осуществляют в барьерном разряде. [6]
Искровой характер микроразрядов подтверждается характерным звуком ( шипением) барьерного разряда. [7]
Важнейшей и наиболее изученной в настоящее время реакцией в барьерном разряде является синтез озона из кислорода, в связи с которым приборы для проведения реакций в барьерном разряде обычно и называются озонаторами. [8]
В заключение данного параграфа следует отметить, что характеры химического действия барьерного разряда и описанного в § 1 коронного разряда близки, это соответствует их сходству и по остальным признакам. [9]
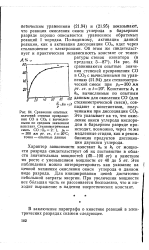 |
Сравнение опытных значений степени превращения СО в СО2 с вычисленными по средним значениям констант. Стехиометрическая смесь СО. О2 2. 1, ро 300 мм рт. ст., t 20 C. точки - опытные данные. [10] |
Фическим уравнениям (21.94) и (21.95) показывают, что реакция окисления окиси углерода в барьерном разряде хорошо описывается уравнением обратимых реакций I порядка. По-видимому, активация данной реакции, как и активация диссоциации СО2, идет через столкновение с электронами. [11]
Известно также активирующее действие аргона и паров воды на реакцию образования перекиси водорода в барьерном разряде. Эти добавки также, вероятно, являются энергетическими катализаторами и влияют на диссоциацию молекул водорода. [12]
Изучение окисления азота [8, 9], синтеза аммиака в тлеющем разряде [10] и образование озона в барьерном разряде [ И ] показывает, что химические процессы в электрическом разряде во многих случаях представляют совокупность гомогенного и гетерогенного процессов, протекающих в объеме и на стенках разрядной трубки. Аналогичная зависимость от расстояния между электродами в озонаторе получается также при анализе данных работы [11] по синтезу озона в барьерном разряде. [13]
В заключение этой серии работ авторы высказывают гипотетические соображения о механизме образования перекиси водорода в барьерном разряде. [14]
Однако модификация полимеров с высокими значениями энергии связи и активации, таких как ПЭНД, в барьерном разряде происходит не полностью или вообще отсутствует. При переходе же к тлеющему разряду при пониженном давлении температура электронов, значительно превышая среднюю температуру газа, достигает десятков тысяч градусов при температуре газа, измеряемой десятками и сотнями градусов. Судя по вращательной, колебательной и электронной температурам газа в барьерном и тлеющем разрядах [ IV.9 ], интенсивность обработки поверхности полимеров в тлеющем разряде должна быть значительно выше, чем в барьерном. [15]
Страницы: 1 2 3 4
