Найденная величина - энергия
Cтраница 1
Найденные величины энергий двух низших состояний хорошо согласуются с экспериментальными значениями, которые равны 4 9 и 6 0 эв. [1]
Найденные величины энергий активации ( Е) неингибированного водородом пиролиза СН по реакции ( I) ( по зависимости k от температуры) составляют для расплавов меди, чугуна и олова соответственно 83000, 68500 и 74800 кал / моль. Расчет величины Е для глубокого пиролиза метана, как для реакции первого порядка, приводит к заниженным значениям и существенному непостоянству Е, особенно в областях высоких температур. Таким образом, учет зависимости торможения водородом пиролиза СН4 при расчете Е при больших глубинах превращения метана является обязательным. Полученные значения Е меньше энергии активации чисто гомогенного процесса, для которого Е 101 500 кал / моль, такое торможение пиролиза свидетельствует о значительной гетерогенной составляющей процесса. [2]
Найденную величину энергии активации соответственно выбору числа т следует рассматривать как близкую к верхнему пределу истинного значения. При меньшем числе степеней свободы последнее может быть ниже на несколько ккал / моль. [3]
Сравнение найденных величин энергии активации в различных интервалах температур с теплотой образования комплекса Вг2 - С6Ню ДЯ, позволяет считать, что уравнение ( 2) описывает скорость реакции в области низких температур - 70 -; - - 50 С. [4]
По найденной величине энергии следует определить ожидаемый пробег ( л-мезона и сопоставить этот пробег с шириной поля зрения микроскопа. Треки, длина которых существенно превышает найденный пробег, не могут, очевидно, принадлежать ( г-мезону, какова бы ни была схема ir - ц-распада. [5]
Резкое различие между найденными величинами энергии активации для реакции ароматизации и для реакции образования олефинов ставит под сомнение утверждение Тэплора и Йедданапаллп 30 о толь что большая величина энергии активации реакции Дегидрогенизации циклогексана на окисных катализаторах объясняется большой величиной энергии десорбции водорода в этом случае. Дегидрогенизация, а следовательно, и десорбция водорода с катализатора происходят как при образовании олефинов. Таким образом, резкое различие в величинах кажущейся энергии активации этих двух реакций не может обусловливаться энергией десорбции водорода, а зависит только от различия в механизме этих двух реакций. [6]
В табл. 7 - 14, где приводятся найденные величины энергии, названия веществ, для которых использовались эти значения параметров, отмечены звездочками. [7]
 |
Зависимость логарифма константы ( lg k скорости реакции от обратной температуры ( Т при различном давлении окиси углерода ( Рсо ( в am. [8] |
По данным, определенным из рис. 1, и найденной величине энергии активации были вычислены ( аналогично описанному на стр. [9]
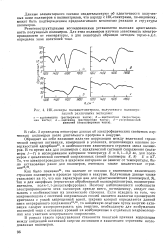 |
ИК-спектры полиацетонитрила, полученного полимеризацией различными методами. [10] |
В рамках такого представления становится понятной причина корреляции между найденной величиной энергии активации и химическим строением исследованных полимеров. [11]
В этом, вероятно, и состоит основная причина корреляции между химическим строением и найденной величиной энергии активации. [12]
При расчете, выполненном для N-бензальанилина, бензальазина и пентафторгуанидина с использованием термохимических данных из работ22 26, получены соответственно следующие значения энергий связи C N: 129, 130 и 132 ккал, подтверждающие реальность найденной величины энергии С М - связи в ксилилендиизопианатах. [13]
Найденная величина энергии резонанса этого вещества, равная 24 ккал / моль, хорошо согласуется с величиной 17 2 ккал / моль, найденной ранее в § 3.2. Тиофен и пиррол сходны с фураном и, несомненно, их энергии резонанса не очень различны. Из приведенных данных становится ясно, какое влияние оказывают одна или две фенильные группы в индоле и карбазоле. [14]
Хотя это значение более вероятно, чем получаемое спектральными методами ( см. стр. Поэтому найденная величина энергии диссоциации АЮ может содержать значительную ошибку. [15]
Страницы: 1 2