Парциальная величина
Cтраница 3
Если резкая изменчивость парциальных величин § ъ о, отмеченная в главе VIII. [31]
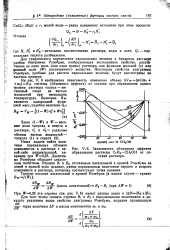 |
Зависимость объемного эффекта образования раствора С7Н8 - СН3ОН от состава раствора. [32] |
Для графического определения парциальных величин в бинарном растворе удобна диаграмма Розебума, изображающая экстенсивное свойство, рассчТй - танное на один моль ( или один грамм) раствора, как функцию мольной ( х) или весовой доли ( W) растворенного вещества. Некоторые свойства диаграммы Розебума, удобные для расчета парциальных величин, будут рассмотрены на частном примере. [33]
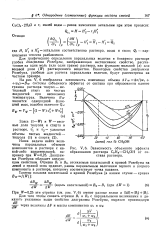 |
Зависимость объемного эффекта образования раствора С Нз - СН3ОН от состава раствора. [34] |
Для графического определения парциальных величин в бинарном растворе удобна диаграмма Розебума, изображающая экстенсивное свойство, рассчитанное на один моль ( или один грамм) раствора, как функцию мольной ( х) или весовой доли ( W) растворенного вещества. Некоторые свойства диаграммы Розебума, удобные для расчета парциальных величин, будут рассмотрены на частном примере. [35]
Химический потенциал является парциальной величиной, и вывод о возможности пяти типов граничного хода парциальных величин в двухкомпонентном растворе ( см. рис. 1.1) приложим и к химическому потенциалу. [36]
ДЯ и AS - парциальные величины, зависящие от концентрации. [37]
Следует подчеркнуть, что парциальные величины отличны от химических потенциалов, поскольку для химического потенциала производная берется при постоянных естественных переменных, а в случае парциальных величин - при постоянных температуре и давлении. [38]
В идеальном растворе эти парциальные величины являются функциями температуры и давления, но явно не зависят от природы и количества других компонентов. [39]
В области разбавленных растворов парциальные величины макрокомпонента близки к мольным значениям чистого макрокомпонента. [40]
Парциальные давления не являются парциальными величинами с точки зрения указанного определения и не обладают соответствующими математическими свойствами. [41]
В случае идеальных растворов такие парциальные величины, как энтальпия, объем, теплоемкость, остаются такими же, как и для чистых жидкостей. Поэтому можно думать, что в реальных системах, содержащих один из компонентов в малых количествах, эти парциальные величины для обоих компонентов испытывают малое возмущение. [42]
Из (11.97) следует, что парциальные величины тех или иных экстенсивных свойств системы есть величины интенсивные. В частности, интенсивной величиной является химический потенциал ц, который вследствие этого должен определяться также интенсивными величинами. [43]
С-С, a lfpq - эффективная парциальная величина, соответствующая связи этого вида. [44]
Легко показать, что для парциальных величин справедливы все дифференциальные уравнения термодинамики. [45]
Страницы: 1 2 3