Распад - олефин
Cтраница 2
Представляет большой интерес работа [23] по изучению взаимного влияния при пиролизе различных смесей парафиновых и оле-1 финовых углеводородов. В этой работе показано, что влияние углеводородов в процессе на скорость превращения противополож-I но: олефин ингибирует распад парафина, а парафин ускоряет распад олефина. Наибольшее ингибирующее действие олефйнов наблюдается в системе этан-олефин. При пиролизе высших парафиновых углеводородов взаимное влияние углеводородов на скорость превращения значительно слабее) Хак, при пиролизе пропд-лена в при утст и эта на реакция р х: & адд полностью направлена в - стоуону образования этилена и метана. Эти весьма интересные наблюдения могут-я виться основой для дальнейшего раавитая ра бот, направленных на регулирование состава продуктов пиролиза жидкого сырья в присутствии этана. [16]
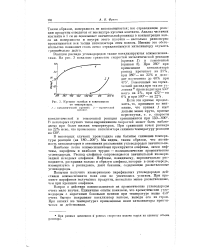 |
Крекинг газойля в зависимости от температуры. [17] |
Мы видим, таким образом, что активность катализаторов в отношении разложения углеводородов значительна. Наиболее легко алюмосиликатами крекируются олефины, затем наф-тены, парафины и наиболее трудно - полициклические ароматические углеводороды. Распад олефинов сопровождается значительной изомеризацией исходных олефинов. Нафтены, повидимому, первоначально распадаются, раскрывая кольцо и образуя олефины, которые в свою очередь, изомеризуясь и распадаясь, дают бензины, содержащие разветвленные углеводороды. [18]
В работах, посвященных изучению механизма крекинга углеводородов, В. В. Воеводский впервые предположил, что крекинг олефинов протекает цепным путем, и выдвинул цепную схему, включающую новый элементарный акт Кнепр-Ьол - - НПр диен, заключающийся в переходе атома Н от радикала олефина к олефину с образованием алкильного радикала. Гипотеза о цепном характере распада олефинов была впоследствии подтверждена экспериментально. [19]
Энергии разрыва слабейшей средней С-С - связи в молекуле нормальных парафинов составляют: 318 2 кДж / моль ( 76 ккал / моль) в СеНи; 314 кДж / моль ( 75 ккал / моль) в C7Hie и 309 8 кДж / моль ( 74 ккал / моль) в CsHi8 [ 34, с. Связь С-С в молекуле олефи-на, сопряженная с двойной, имеет энергию разрыва около 257 5 кДж / моль ( 61 5 ккал / моль) [ 34, с. Поэтому инициирование цепей в основном происходит не при распаде исходного парафина, а в результате распада олефинов. [20]
Эглофф с сотрудниками [51] показал, что при атмосферном давлении алго-мосиликатный катализатор вызывает распад бутиленов и амиленов при температурах 400 С и выше. Таким образом, в условиях алкилирования, приведенных в работе [54], каталитический распад может предшествовать алки-лированию, когда исходными алкилирующими углеводородами являются не только парафины ( пентан), но и олефины. Более того, на основании данных [51] следует ожидать, что при каталитическом алкшшровании ароматических углеводородов олефинами предварительный распад олефинов будет происходить в большей степени, чем при каталитическом алкилировании парафинами, так как оптимальная температура распада олефинов значительно ниже температуры распада соответствующих парафинов. Следовательно, в работе Саханена и О Келли [54] образование алкилароматических углеводородов с короткими боковыми цепями обусловлено не только крекингом боковых цепей, получившихся при алкилировании алкилароматических углеводородов с длинными боковыми цепями, но и алкилировапием низкомолекулярными продуктами распада олефинов. [21]
В этом случае наличие предела торможения объясняется переходом от развития цепи в реакции с участием активных радикалов к развитию цепи с участием радикалов типа аллильных. По мере увеличения числа групп СН3 в молекуле добавляемого в процессе олефина эффект торможения распада низкомолекулярных парафиновых углеводородов до определенного предела возрастает, а затем падает. Наличие максимума на кривой торможения процесса распада объясняется взаимодействием олефина вначале с активными радикалами, в результате чего их количество в зоне реакции снижается, в дальнейшем при распаде олефина образуется молекула ингибитора ( например, пропилена), в связи с чем эффект торможения процесса распада повышается еще в большей степени. При добавке более высокомолекулярных разветвленных олефинов ( например, тетраметилэтилена) распад парафиновых углеводородов ускоряется, так как в этом случае при распаде олефина образуется больше активных, чем малоактивных радикалов. С увеличением температуры тормозящий эффект ингибиторов уменьшается. [22]
Эглофф с сотрудниками [51] показал, что при атмосферном давлении алго-мосиликатный катализатор вызывает распад бутиленов и амиленов при температурах 400 С и выше. Таким образом, в условиях алкилирования, приведенных в работе [54], каталитический распад может предшествовать алки-лированию, когда исходными алкилирующими углеводородами являются не только парафины ( пентан), но и олефины. Более того, на основании данных [51] следует ожидать, что при каталитическом алкшшровании ароматических углеводородов олефинами предварительный распад олефинов будет происходить в большей степени, чем при каталитическом алкилировании парафинами, так как оптимальная температура распада олефинов значительно ниже температуры распада соответствующих парафинов. Следовательно, в работе Саханена и О Келли [54] образование алкилароматических углеводородов с короткими боковыми цепями обусловлено не только крекингом боковых цепей, получившихся при алкилировании алкилароматических углеводородов с длинными боковыми цепями, но и алкилировапием низкомолекулярными продуктами распада олефинов. [23]
Алкилирование всегда сопровождается процессами полимеризации, которые подавляются по мере увеличения избытка изопарафина. Изобутан - самый важный компонент парафинового алкилирования - содержится в природных газах и в газах нефтеочистки в гораздо меньшем количестве, чем бутан. Поэтому фракции бутана часто изомеризуют в изобутан в присутствии хлористого алюминия. Кроме того, можно алкилирование объединить с полимеризацией, так как вследствие распада олефинов изобутан оказывается уже сконцентрированным. [24]
В этом случае наличие предела торможения объясняется переходом от развития цепи в реакции с участием активных радикалов к развитию цепи с участием радикалов типа аллильных. По мере увеличения числа групп СН3 в молекуле добавляемого в процессе олефина эффект торможения распада низкомолекулярных парафиновых углеводородов до определенного предела возрастает, а затем падает. Наличие максимума на кривой торможения процесса распада объясняется взаимодействием олефина вначале с активными радикалами, в результате чего их количество в зоне реакции снижается, в дальнейшем при распаде олефина образуется молекула ингибитора ( например, пропилена), в связи с чем эффект торможения процесса распада повышается еще в большей степени. При добавке более высокомолекулярных разветвленных олефинов ( например, тетраметилэтилена) распад парафиновых углеводородов ускоряется, так как в этом случае при распаде олефина образуется больше активных, чем малоактивных радикалов. С увеличением температуры тормозящий эффект ингибиторов уменьшается. [25]
Эглофф с сотрудниками [51] показал, что при атмосферном давлении алго-мосиликатный катализатор вызывает распад бутиленов и амиленов при температурах 400 С и выше. Таким образом, в условиях алкилирования, приведенных в работе [54], каталитический распад может предшествовать алки-лированию, когда исходными алкилирующими углеводородами являются не только парафины ( пентан), но и олефины. Более того, на основании данных [51] следует ожидать, что при каталитическом алкшшровании ароматических углеводородов олефинами предварительный распад олефинов будет происходить в большей степени, чем при каталитическом алкилировании парафинами, так как оптимальная температура распада олефинов значительно ниже температуры распада соответствующих парафинов. Следовательно, в работе Саханена и О Келли [54] образование алкилароматических углеводородов с короткими боковыми цепями обусловлено не только крекингом боковых цепей, получившихся при алкилировании алкилароматических углеводородов с длинными боковыми цепями, но и алкилировапием низкомолекулярными продуктами распада олефинов. [26]
Страницы: 1 2