Распад - перекисное соединение
Cтраница 1
Распад перекисных соединений и его характер в большой степени определяются внешними факторами воздействия. Большое влияние оказывает растворитель. [1]
Распад перекисных соединений изучается давно. Для многих целей важным является изучение скорости термического распада, конечных продуктов превращения и механизма этого распада, а также влияния на распад различных условий: температуры, растворителей и, особенно, положительных и отрицательных катализаторов. Распад перекисных соединений различного строения протекает по-разному. [2]
Поэтому распад перекисных соединений почти не затрагивает главных цепей; имеет место отщепление формальдегида или муравьиной кислоты, если в этом распаде участвует вода. [3]
Продукты распада перекисных соединений этилена представляют собой активные радикалы. С образования их и начинается процесс цепной радикальной полимеризации. [4]
На скорость распада перекисных соединений в водной среде значительно влияет наличие в реакционной системе эмульгаторов, причем это влияние зависит от природы и концентрации эмульгатора, а также от рН среды. Ускоряющее влияние на распад инициаторов усиливается при увеличении концентрации эмульгаторов. Однако в более поздних работах Кольтгофф и сотрудники [46, 56], указывают, что ускоряющего влияния спиртов и эмульгаторов на распад персульфата калия при наличии мономеров не наблюдается. Авторы делают вывод, что образующиеся при распаде персульфата сульфатные радикалы быстрее реагируют с двойной связью мономера, чем со спиртами. [5]
 |
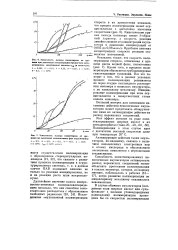
Зависимость процесса полимеризации от концентрации инициатора Н2О2. [6] |
В этом случае распад перекисных соединений на свободные радикалы ( Fe2 - H2O2 - HFe3 OH - - f ОН -) происходит при пониженной температуре, так как требует меньшей затраты энергии. [7]
Хемилюминесценция в реакциях катализированного распада перекисных соединений исследовалась более подробно. [8]
Способность оксиэтилированных неионогенных эмульгаторов активировать распад перекисных соединений может объяснять протекание полимеризации в каплях мономера, которое, по нашему мнению, наблюдалось в работах [13- 17], когда развитие полимеризации по мицеллярному механизму оказывалось невозможным. [10]
К реакциям, которые инициируются распадом перекисных соединений и протекают с промежуточным образованием свободных радикалов, относятся полимеризация олефинов и присоединение по двойной связи, которые будут описаны позже. [11]
Способность оксиэтилиров энных неионогенных эмульгаторов активировать распад перекисных соединений может объяснять протекание полимеризации в каплях мономера, которое, по нашему мнению, наблюдалось в работах [13- 17], когда развитие полимеризации по мицеллярному механизму оказывалось невозможным. [13]
Следует подчеркнуть, что задача предотвращения распада перекисных соединений и накопление их в максимальных количествах является принципиальным отличием данного процесса от многочисленных процессов окисления углеводородов, описанных в литературе. [14]
Полагают, что наиболее вероятной причиной взрыва явился распад перекисных соединений производных ацетилена в результате подачи в коллектор нефлегматизированного ацетилена и возможного подсоса воздуха через неплотности при сливе воды из скруббера. [15]
Страницы: 1 2 3