Распад - соль
Cтраница 2
Концентрация COz в паре складывается из первичной СС2, образующейся в результате распада солей, и вторичной СО2, внесенной в пар с неконденсирующимися газами, выведенными из паровой полости греющих секций и соответствующих подогревателей. [16]
 |
Зависимость скорости коррозии различ. [17] |
Нержавеющие стали обладают хорошей стойкостью к большинству солей до тех пор, пока распад солей не приводит к образованию критических концентраций соответствующих кислот. Исключением являются соли галоидоводородных кислот, которые в определенных условиях сами могут вызвать питтинговую коррозию. Соли хлорноватистой кислоты особенно способны приводить к питтингообразованию, и поэтому не следует допускать продолжительных контактов с такими солями. [18]
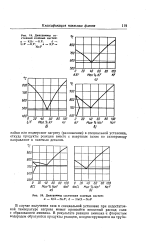 |
Диаграммы состояния солевых систем.| Диаграммы состояния солевых систем. [19] |
В случае получения газа в специальной установке при недостаточной температуре нагрева может произойти неполный распад соли с образованием аммиака. [20]
В случае получения газа в специальной установке при недостаточной температуре нагрева может произойти неполный распад соли с образованием аммиака. В результате реакции аммиака с фтористым водородом образуются продукты реакции, конденсирующиеся на трубопроводах и засоряющие их. По этой причине образование аммиака допускать не следует. Количество солйй, необходимых для получения газового флюса, зависит от многих причин, поэтому обычно его подбирают опытным путем. [21]
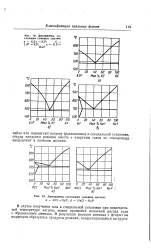 |
Диаграммы состояния солевых систем.| Диаграммы состояния солевых систем. [22] |
В случае получения газа в специальной установке при недостаточной температуре нагрева может произойти неполный распад соли с образованием аммиака. [23]
Обычно считают, что миграция карбоксилатной группы в солях таких кислот является результатом предварительного распада соли на фенолят и угольный ангидрид. [24]
Примером реакции, в промежуточной стадии которой образуются ионы карбония, может служить реакция распада солей диазония. Известно, что соли диазонил способны восстанавливаться до углеводородов спиртами, фосфорнозатистой кислотой и некоторыми другими соединениями. Корнблюм [74] показал, что восстановление фосфорноватистой кислотой солей диазония имеет радикально-цепной механизм. Исследуя механизм восстановления солей диазония спиртами, Рекашева и Миклухин [75, 76] показали, что восстановление происходит в результате перемещения атома водорода от углерода, а не от кислорода, так как образовавшийся в результате реакции с дейтероэтанолом ароматический углеводород не содержал дейтерия. [25]
Образующиеся при этом галоидоводороды оказывают такое же действие на окислы, как и в изолированном виде или при распаде солей аммония. Преимущество органических комплексных соединений перед неорганическими заключается в их меньшей коррозионной активности. Из многообразия потенциально возможных органических комплексных солей для пайки применяются только некоторые. [26]
Интересно отметить, что при проведении реакции в среде четыреххлористого углерода ни перекись ацетила, ни УФ-облучение не инициировали распада соли свинца; наблюдалось лишь ее медленное термическое разложение. [27]
Наконец, в связи с дпазомотодом Несмеянова, как своеобразное дополнение к нему, был открыт ( А. Н. Несмеяновым и О. А. Реутовым) распад арилазокарбоновых солей под влиянием сулемы в среде ацетона. [28]
Химические способы борьбы основаны на изучении причин выпадения солей из пластовых вод и применении различных реагентов, приводящих к торможению процесса распада солей. [29]
Интересно, что в качестве побочного продукта реакции в этом случае был выделен метиловый эфир ( 3-нафтола, который, повидимому, образуется путем распада соли четвертичного аммониевого основания до ( i-нафтола с последующим его метилированием. [30]
Страницы: 1 2 3