Распад - углеводород
Cтраница 1
Распад углеводородов в жидкой фазе гидрогенизации должен рассматриваться как гомогенный некаталитический процесс. [1]
Распад углеводородов на радика лы ( инициирование цепи) осуществляется преимущественно по связи С-С. Разрыва С - Н - связи не происходит, так как для этого требуется значительно больше энергии: энергия С-С - связи 360 кДж / № оль; энергия С - Н - связи 412 кДж / моль. [2]
Включает одновременный распад углеводородов и хлорирование молекулярных фрагментов. [3]
Процесс распада углеводородов под действием A1CL, протекающий с изомеризацией, принято называть деструктивным алкилп-рованпсм. [4]
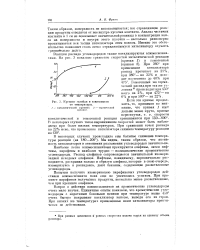 |
Крекинг газойля в зависимости от температуры. [5] |
Реакции распада углеводородов также катализируются алюмосиликатами. [6]
Реакция распада углеводородов олефинового ряда в некоторых случаях сопровождается конденсацией олефинов и циклизацией их в нафтены. [7]
Для предотвращения распада углеводорода на элементы необходимо вести процесс так, чтобы первые реакции были приостановлены до достижения термодинамического равновесия. [8]
 |
Результаты исследования каталитического крекинга. [9] |
При каталитическом крекинге распад углеводорода и образование газообразных и низкокипящих жидких продуктов происходит значительно интенсивнее, чем при термическом крекинге в тех же условиях температуры и давления. При действии высокого давления, как уже неоднократно отмечалось, преобладают процессы, протекающие с уменьшением объема реакционной среды. Для частного случая крекинга углеводородов таковыми являются: алкилирование, гидрирование, полимеризация. [10]
Например, при распаде углеводородов активной частицей являются алкильные радикалы, которые могут реагировать с окисью азота по уравнению СНз - j - NO - - H20 HCN. Эта реакция приводит к обрыву цепи и торможению реакций распада, что снижает скорость реакции в десятки раз. [11]
Например, при распаде углеводородов активной частицей являются алкильные радикалы, которые могут реагировать с оксидом азота по уравнению - СН3 NO - - Н2О HCN. Эта реакция приводит к обрыву цепи и торможению реакций распада, что снижает скорость реакции в десятки раз. [12]
Например, при распаде углеводородов активной частицей являются алкильные радикалы, которые могут реагировать с оксидом азота по уравнению - СН3 NO - H2O HCN. Эта реакция приводит к обрыву цепи и торможению реакций распада, что снижает скорость реакции в десятки раз. [13]
В ядре пламени происходит распад углеводорода на углерод и водород. Распыленный углерод придает этой зоне яркое свечение. [14]
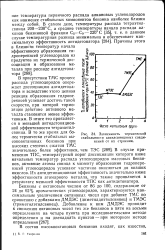 |
Зависимость термической стабильности алкилсвинцовых соединений от их строения. [15] |
Страницы: 1 2 3 4