Гомолитический распад
Cтраница 1
Гомолитический распад начинается с разрыва О-О - связи. [1]
При гомолитическом распаде Н2 степень окисления иона металла изменяется. [2]
При старении полиимидов происходит гомолитический распад имидного цикла, причем энергии активации процесса старения, рассчитанные по температурным зависимостям коэффициентов а и ( имеют близкие значения: f / e 159 6 4 2 кДж / моль и [ / 159 6 12 6 кДж / моль. [3]
Этим объясняется сравнительная легкость гомолитического распада меркаптанов по сравнению с аналогичными спиртами. [4]
В противоположность ароматическим аналогам большинство алифатических азосоединений относительно непрочно и претерпевает гомолитический распад под влиянием тепла и света. Лабильность алифатических азосоединений будет, очевидно, зависеть от природы заместителей; смешанные арил-алкилазосоединения, как и следовало ожидать, являются более стойкими. Газ азометан ( СН3 - N N - СН3) заметно не разлагается до 200 С. Однако, если ввести а-заместители, способные стабилизировать получающиеся свободные радикалы, гомолитический распад происходит легче. Пространственные факторы также могут играть решающую роль, как будет показано на примере циклических и стерически затрудненных азосоединений. [5]
Если взаимодействие полисульфидных олигомеров с мета-крилатами проводится при повышенной температуре, возможен гомолитический распад дисульфидных связей олигомера. Наиболее вероятными являются радикалы типа - RS -, способные взаимодействовать по двойной связи, тогда как тиильные - RSS - радикалы мало активны и не участвуют в реакциях полимеризации. Образование свободных радикалов при отрыве водорода от HS-группы олигомера не является определяющим в этом процессе, поскольку аддукты, получаемые при взаимодействии олигомеркаптанов и метакрилатов, имеют высокую среднечисленную функциональность. [7]
Реакции окислительного старения начинаются при значительно более низких температурах, чем реакции чисто термического гомолитического распада. Уже при комнатной температуре признаки деструкции обнаруживают у некоторых материалов, особенно если они не защищены от окисления. Поэтому окислительные реакции - значительно более важный фактор старения полимерных материалов, чем термическое разложение. [8]
Ллойд предположил, что ион металла и перекись образуют комплекс путем реакции, конкурирующей с обычным гомолитическим распадом перекиси. Поскольку молекулярный вес возрастает, а число концевых групп уменьшается, автокатализ приобретает основное значение. [9]
К реакциям замещения нитрильной группы можно формально отнести некоторые описанные в литературе реакции, основанные на гомолитическом распаде дициана. При взаимодействии ди-циана и молекулярного водорода при 550 С образуется цианистый водород. [10]
Некоторые авторы считают, что в каталитической системе, содержащей Ti4, во время его восстановления при гомолитическом распаде неустойчивых титанорга-нических соединений возникают свободные радикалы или ион-радикалы, которые инициируют полимеризацию олефинов. Адсорбированный алкильный радикал в ходе реакции роста движется вдоль поверхности и присоединяет адсорбированные молекулы мономера, причем, будучи локализованными на поверхности, эти радикалы не подвергаются столь быстрой гибели за счет бимолекулярного обрыва, как свободные радикалы. [11]
Поэтому первой и определяющей общую скорость реакции стадией при вулканизации в присутствии М 1Ч - диэтилбензтиазил-2 - сульфен-амида следует считать гомолитический распад ускорителя на радикалы 2-бензтиазила и диэтиламина. Такие активные осколки могут при радикальной реакции дегидрировать каучук, причем вновь образуются 2-меркаптобензтиазол и диэтиламин. Меркаптобензти-азол в свою очередь может реагировать с кольцом серы S8, которое раскрывается с образованием радикалов. Каждая молекула NjN - ди-бензтиазил-2 - сульфенамида может, следовательно, привести к образованию двух радикалов каучуковой цепи, которые реагируют с серой, давая серные мостики, или способствуют образованию активной серы. [12]
Их каталитическая активность по отношению к реакциям окисления - восстановления обусловливается наличием на их поверхности свободных электронов, способствующих адсорбции, хемосорбции, гомолитическому распаду органических молекул. [13]
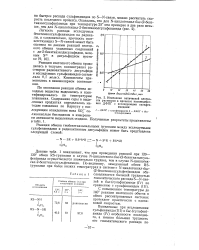 |
Изменение оптической плотно -, сти растворов в процессе взаимодействия ДФПГ с исследуемыми сульфенамидами. [14] |
Выявленные при исследовании сульфенамида ( III) иб с - ( сульфен) - амида ( IV) особенности последнего, а именно большая трудность его гомолитического распада по. [15]
Страницы: 1 2