Расположение - связь
Cтраница 3
Несмотря на то что расположение связей в аминах приближается к тет-раэдрической конфигурации ( неподеленная пара электронов эквивалентна одной связи), ни один обычный третичный амин не был расщеплен на энантиомеры. В молекулах этого типа две энантиомерные формы амина очень быстро переходят друг в друга, причем неподеленная пара электронов в известном смысле слова проходит через атом азота. [31]
Если предположить, что расположение связей атомов металла должно быть таким, что шесть окружающих атомоз или групп будут находиться на равном расстоянии от центрального атома, а такж:, ч го кратчайшие расстояния А - А все одинаковы, как это следует ожшать для симметричного комплекса СоА6, то формулами правильного октаэдра будут плоский шестиугольник и тригональная призма. [32]
В табл. 10 представлено расположение связей атомов хлора в различных изомерах 1 2 3 4 5 6-гексахлор-циклогексана. [33]
 |
Схема, показывающая образование химических связей в молекуле С Н. [ IMAGE ] Схема, показывающая образование химических связей в молекуле С Н. [34] |
На рис. 1.44 схематически изображено расположение связей в молекуле ацетилена НС СН. В данной молекуле только два электрона углеродного атома образуют гибридные орбитали - происходит sp - гибридизация. [35]
 |
Схема образования химических связей в молекуле СОг. [36] |
На рис. 1.41 схематически изображено расположение связей в молекуле ацетилена НС СН. В данной молекуле только две орбитали углеродного атома образуют гибридные орбитали - происходит sp - гибридизация. Молекула СгШ имеет линейную структуру. Две р-орбитали атома углерода, оставшиеся негибридизованными, располагаются под углом 90е друг к другу. [37]
 |
Схема образования химических связей в молекуле СОг. [38] |
На рис. 1.41 схематически изображено расположение связей в молекуле ацетилена НССН. В данной молекуле только две орбитали углеродного атома образуют гибридные орбитали - происходит sp - гибридизация. Молекула CjHi имеет линейную структуру. Две р-орбитали атома углерода, оставшиеся негибридизованными, располагаются под углом 90 друг к другу. [39]
 |
Схема, показывающая образование химических связей в молекуле. [40] |
На рис. 82 схематически изображено расположение связей в молекуле ацетилена НССН. В данном случае только два электрона углеродного атома образуют гибридные орбитали - происходит sp - гибридизация. Молекула С2Н2 имеет линейную структуру. Две р-орбитали атома углерода, оставшиеся негибридизирован-ными, располагаются под углом 90 друг к другу. Эти орбитали образуют две л-связи, электронные облака которых располагаются около двух взаимно перпендикулярных плоскостей. [41]
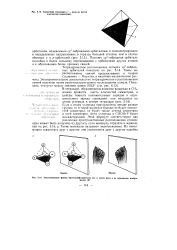 |
Симметрия тетраэдра ( 7 - одна из шести плоскостей симметрии.| Энантиоиерные формы бромхлорфторметана ( а и левая рука и ее зеркальное изображение ( б. [42] |
Такое же коричные р6и мм расположение связей предсказывают и теория Сиджвика - Пауэлла, и квантово-механические расчеты. Экспериментальное доказательство тетраэдрического расположения связей получено путем рентгеноструктурного исследования алмаза. [43]
 |
Схема, показывающая образование химических связей в молекуле С Н. [ IMAGE ] Схема, показывающая образование химических связей в молекуле С Н. [44] |
На рис. 1.44 схематически изображено расположение связей в молекуле ацетилена HCsCH. В данной молекуле только два электрона углеродного атома образуют гибридные орбитали - происходит sp - гибридизация. [45]
Страницы: 1 2 3 4 5