Регулярное расположение - атом
Cтраница 2
Другим важным отличием реальной кристаллической решетки от упрощенной идеализированной модели является существование линейных дефектов или дислокаций. В обоих случаях дислокации нарушают регулярное расположение атомов кристаллической решетки. [16]
Что касается поверхностной теории, то с ее позиций - растворимый кремнезем представляет собой несущественную, случайную форму, тогда как именно поверхность, или граница, раздела фаз кварцевой частицы способна вызывать изменения в органических молекулах. Основная идея заключается в том, что регулярное расположение атомов на поверхности кристаллической решетки действует как матрица, по которой совмещаются полярные группы белковых молекул. Последние таким образом могут адсорбироваться и затем модифицироваться. В теории иммунной реакции, которая не вступает в противоречие с другими теориями, делается попытка объяснить последующие этапы при развитии силикозных повреждений. [17]
На идеально чистой поверхности происходит внезапный обрыв регулярного расположения атомов. Координация атомов на поверхности должна быть иной, чем координация в объеме. Это справедливо как для ковалентной связи, так и для чисто ионных решеток. Следовательно, атомы на поверхности должны иметь ненасыщенные связи, способные реагировать с другими элементами или соединениями. Прочности таким образом образовавшихся связей с другими элементами, отличающимися от элементов основной структуры, могут изменяться в широких пределах. Говорить об истинном поверхностном соединении можно только в том случае, если характер связи на поверхности аналогичен характеру связи внутри структуры и если прочность того же порядка, что и в химических соединениях. [18]
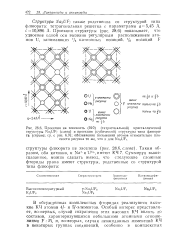
Структура NazUF7 также родственна со структурой типа флюорита: тетрагональная решетка с параметрами а 5 45 А, с10 896 А. Проекция структуры ( рис. 28.6) показывает, что удвоение одной оси вызвано регулярным расположением атомов U, занимающих / 4 катионных позиций. [20]
Кристалличность зависит от химического строения, которое, в свою очередь, оказывает влияние па силы межмолекулярного взаимодействия. Системы водородных связей, сильно полярные группы, легко ионизирующиеся сегменты - это те точки, в которых осуществляется притяжение между молекулярными цепями, обусловливающее кристалличность высокополимера. Регулярное расположение атомов или групп, определяющих межмолекулярные силы, более предпочтительно, так как при этом обеспечиваются наилучшие условия для полного проявления действия этих сил. Важную роль играют также пространственные факторы. [21]
Стабильность молекулы зависит от химических связей ее атомов. Как упоминалось раньше, именно квантовая физика пролила свет на первоначально весьма туманную природу химических связей. Кристалл ( подобный алмазу) является регулярным расположением атомов ( атомов углерода в случае алмаза), периодическим в трех независимых пространственных направлениях. Здесь связи распространяются между всеми атомами, и таким образом кристалл является единственной молекулой. Стабильность твердых тел является стабильностью кристаллов, и если модель Дельбрука в основном верна, то стабильность генов основывается на тех же квантовомеханических основах. Однако, в то время как в кристалле те же самые строительные кирпичи повторяются периодически, каждый атом в гене имеет свои специфические неизменяемые место и роль. Однако Шредингер говорит о гене как об апериодическом кристалле и приписывает ему высшую степень порядка и организации, чем у периодического кристалла. [22]
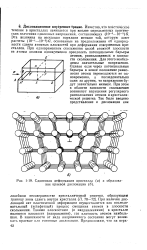 |
Сдвиговая деформация кристалла ( а и образование краевой дислокации ( б. [23] |
Для этого необходимы значительные напряжения. Однако если через потенциальные барьеры в новое положение равновесия атомы перемещаются не одновременно, а последовательно один за другим, то напряжения будут значительно меньше. При этом в области плоскости скольжения возникнут нарушения регулярного расположения атомов в кристаллической решетке. [24]
Предположив, что 6 углеродных атомов бензольного кольца образуют симметричный шестиугольник, легко было прийти к выводу, что все шесть атомов водорода равноценны. Например, не играет роли, у какого атома углерода - первого, второго, третьего или пятого - произошло замещение атома водорода на атом хлора, поскольку все атомы водорода одинаково расположены в пространстве и имеют одинаковые связи. Тот факт, что у однозамещенных производных бензола отсутствует изомерия, вполне может служить доказательством регулярного расположения атомов углерода в шестиугольнике бензола. [25]
Ферромагнетизм наблюдается в Зс. Так как все перечисленные вещества являются кристаллическими, можно было бы предположить, что для параллельного упорядочения магнитных моментов необходимо наличие регулярного расположения атомов. [26]
Полимеры, пригодные для получения синтетических волокон, должны обладать определенной степенью упорядоченности структуры ( кристалличности) и сохранять ее в вытянутом состоянии. Кристалличность полимера зависит от его химического строения. Особенно благоприятно сказываются сильно полярные группы, водородные связи, через которые осуществляется притяжение между молекулярными цепями, обусловливающее кристалличность полимера. Регулярное расположение атомов или групп, определяющих межмолекулярные силы, обеспечивает более полное проявление действия этих сил. [27]
В тех случаях, когда нужно было учитывать межмолекулярное взаимодействие, оно рассматривалось как некоторое возмущение. Такой подход становится, вообще говоря, неприемлемым при рассмотрении кристаллов. В кристаллах атомы, молекулы или ионы1) расположены на малых расстояниях друг от друга и не могут значительно смещаться от своих средних положений. Межмолекулярные силы при этом не могут считаться малыми, так как ими, по существу, обусловлено само существование кристалла. Далее, кристаллы характеризуются регулярным расположением атомов и соответственно слмметрией. Эта симметрия в значительной степени определяет все свойства кристалла. [28]
Страницы: 1 2