Рассмотрение - электронное строение
Cтраница 1
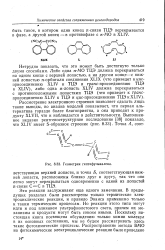 |
Геометрия гептафульвалена. [1] |
Рассмотрение электронного строения позволяет сделать лишь такие выводы, но анализ моделей показывает, что первая альтернатива - гораздо более благоприятна, а она приводит к продукту XLVII, что и наблюдается в действительности. [2]
Метод рассмотрения электронного строения молекулы бензола типичен для изучения непредельных органических соединений. Обычно а-связи атомов углерода описываются в рамках метода ВС с помощью подходящих гибридных орбиталей, а я-связи рассматриваются в рамках метода МО. Такой подход оправдан тем, что сг-связывающие орби-тали обычно значительно устойчивей, поэтому электроны на я-орбита-лях определяют химические и спектральные свойства молекулы. [3]
Метод рассмотрения электронного строения молекулы бензола типичен для изучения непредельных органических соединений. Обычно а-связи атомов углерода описываются в рамках метода ВС с помощью подходящих гибридных орбиталей, а я-связи рассматриваются в рамках метода МО. Такой подход оправдан тем, что ст-связывающие орби-тали обычно значительно устойчивей, поэтому электроны на л-орбита-лях определяют химические и спектральные свойства молекулы. [4]
При рассмотрении электронного строения молекул, состоящих из атомов с относительно небольшими порядковыми номерами ( например, Z 54) в периодической таблице Д.И. Менделеева, можно исходить из нерелятивистского оператора Гамильтона (2.13), который явным образом не зависит от спиновых переменных. [5]
При рассмотрении электронного строения ферроцена следует учитывать только Зй-и 45-орбиты атома железа. На этих орбитах имеется всего восемь электронов. Если принять атом железа за начало координат, а плоскость ху провести параллельно кольцам циклопентадиенила через атом железа, то в этой п / - плоскости будет две З - орбиты, а именно орбиты 3d & - y и 3dxy, и каждая из них содержит по два электрона. Что касается орбит 3dyz и 3dxz, то на них имеется по одному электрону, и симметрия этих орбит такова, ч то позволяет им образовывать связь с П - орбитами циклопентадиенила. [6]
При рассмотрении электронного строения молекулы СО ( см. разд. [7]
 |
Схема возмущения первого порядка при взаимодействии орбиталей с равными энергиями ( а и возмущение второго порядка при взаимо-действии орСипалеи, сильно различающихся по энергии ( б. [8] |
При рассмотрении электронного строения многоатомных молекул обычно используется один из двух подходов. Согласно одному из них, рассматривается взаимодействие пар атомных орбиталей с образованием локализованных двухцентровых орбиталей. [9]
При рассмотрении электронного строения молекулы СО ( см. разд. Это иллюстрирует также рис. 3.20, показывающий, что энтропии обоих веществ в кристаллическом, жидком и газообразном состояниях при одной и той же температуре почти не отличаются. [10]
При рассмотрении электронного строения молекулы СО ( см. разд. [11]
МОЛЕКУЛЯРНЫХ ОРБИТ МЕТОД в квантовой химии - метод рассмотрения электронного строения молекул, в основе к-рого лежит представление, об образовании хим. связей в результате движения всех электронов в поле всех ядер и электронов молекулы. [12]
Более детальная интерпретация и классификация электронных спектров многоатомных молекул связана с рассмотрением электронного строения молекул. [13]
 |
Электродинамический логометр.| Ферродинамические лстометры. [14] |
ЛОКАЛИЗОВАННЫХ ПАР МЕТОД ( метод валентных схем, метод валентных связей) - метод рассмотрения электронного строения молекул, согласно к-рому образование химич. В соответствии с этим электронное строение молекул описывается нек-рым набором валентных схем. [15]
Страницы: 1 2