Рассмотрение - электронная структура
Cтраница 1
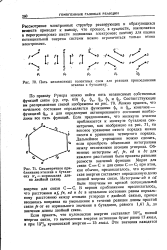 |
Пять независимых валентных схем для реакции присоединения.| Симметричное приближение этилена к бутадиену ( / - нормальная длина двойной связи. [1] |
Рассмотрение электронных структур реагирующих и образующихся веществ приводит к выводу, что процесс, в сущности, заключается в перегруппировке шести подвижных электронов; поэтому для оценки потенциальной энергии системы можно ограничиться только этими электронами. [2]
 |
Влияние симметрии АО при образовании МО. [3] |
Возможность рассмотрения электронной структуры молекул по аналогии с электронной структурой атома основана на общности природы электронов в атомах и молекулах и взаимодействия их с ядрами и друг с другом. [4]
При рассмотрении электронной структуры молекул очень удобно пользоваться простым принципом электронейтральности, согласно которому в устойчивых соединениях каждый атом близок к состоянию электрической нейтральности. Этот принцип подтверждается тем, что для отделения второго, третьего или четвертого электрона от атома необходимо затратить большое количество энергии. [5]
При рассмотрении электронной структуры молекулы СН и других подобных ей молекул гидридов, в которых ядра атомов находятся близко друг к другу, проще начинать с электронной конфигурации объединенного атома. [6]
 |
ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ ( по Некрасову. [7] |
При рассмотрении электронных структур атомов элементов связь системы элементов со строением атомов становится очевидной. [8]
При рассмотрении электронной структуры сэндвичевых комплексов переходных металлов [3] указывалось, что еаг-орбиты бензольных колец по энергии лежат значительно ниже, чем - орбиты цикло-пентадиенильных колец. Это приводит к образованию значительно более прочных б-связей в ареновых комплексах и более сильному оттягиванию электронов с е28 - орбит переходного металла на ареновые кольца по сравнению с циклопентадиенильным комплексом. [9]
Подобного рода рассмотрение электронной структуры атомов редкоземельных элементов дает возможность подойти к объяснению наблюдаемых переходов в состояние аномальной валентности и дает основание предполагать наличие подобного рода аномальной валентности в тех случаях, когда она опытным путем еще не обнаружена. [10]
В МО-методе подход к рассмотрению электронной структуры молекулы близок к тому, которым пользуются в теории атома. Поэтому логично пользоваться для молекулы той же физической моделью, что и для атомов. Электроны движутся в поле ядра и остальных электронов. Полное описание требует введения четвертого квантового числа - спина. [11]
Наиболее общий подход к рассмотрению электронной структуры комплексов связан с расчетами полных волновых функций комплекса как целого ( а не только центрального иона) по методу МО. В области координационных соединений обобщения, полученные на основе метода МО, получили название теории поля лиган-дов. Главная особенность ее состоит в том, что ввиду обычно высокой симметрии координационного узла МО молекулы или иона координационного соединения легко классифицируются по представлениям симметрии и принципиальную схему их образования из орбиталей лигандов можно зачастую построить, не проводя конкретных расчетов. [12]
 |
Тепловое искажение а валентные атомные орбитали. [13] |
Многие теоретические подходы к рассмотрению электронной структуры неупорядоченных материалов так или иначе связаны с моделью молекулярных орбиталей. Возможно, что наиболее близка к ней модель приближения сильной связи, введенная Уэйром и Торпом [260], которая пролила свет на некоторые аспекты, связанные с образованием псевдощели. [14]
Итак, при реализации метода КРЭЯ для рассмотрения электронной структуры кристаллов с локальными центрами необходимо следующее. [15]
Страницы: 1 2