Аммиачный рассол
Cтраница 2
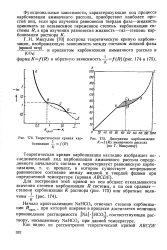 |
Теоретическая кривая карбонизации - f ( R К.| Диаграмма карбонизации. [16] |
Функциональные зависимости, характеризующие ход процесса карбонизации аммиачного рассола, приобретают наиболее простой вид, если при изучении равновесия твердая фаза-жидкость принимать за независимое переменное степень карбонизации системы R, а при изучении равновесия жидкость-газ-степень карбонизации раствора К. [17]
Исследования показывают, что при хранении изолированного-карбонизованного аммиачного рассола равновесное состояние достигается очень медленно. Поэтому методами химического анализа раствора можно определить достаточно точно неравновесные концентрации независимых компонентов [ общ. NHaCOgl при условии, что отбор необходимых для этого двух параллельных проб раствора производится достаточно быстро - в течение 1 мин. [18]
Функциональные зависимости, характеризующие ход процесса карбонизации аммиачного рассола, приобретают наиболее простой вид, если при изучении равновесия твердая фаза - жидкость принимать за независимое переменное степень карбонизации системы R, а при изучении равновесия жидкость - газ - степень карбонизации раствора К. [19]
Исследования показывают, что при хранении изолированного карбонизованного аммиачного рассола равновесное состояние достигается очень медленно. Поэтому методами химического анализа раствора можно определить достаточно точно неравновесные концентрации независимых компонентов [ общ. NHjCO I1 при условии, что отбор необходимых для этого двух параллельных проб раствора производится достаточно быстро - в течение 1 мин. [20]
Приведенная формула позволяет определить выход NaHCO3 при карбонизации аммиачного рассола в практических условиях. [21]
Приведенная формула позволяет определить выход NaHCO - при карбонизации аммиачного рассола в практических условиях. [22]
Кажущаяся простота метода Глууда объясняется тем, что процесс карбонизации аммиачного рассола заменен процессом карбонизации аммиака, с получением кристаллического бикарбоната аммония. [23]
Условия работы карбонизационных колонн и вакуум-фильтров определяют выход NaHCO3 из аммиачного рассола и, следовательно, объем жидкостей. Снижение объемов жидкостей достигается за счет строгого соблюдения норм технологического режима процесса карбонизации. Существенное значение имеет повышение концентрации СО2 в газе известково-обжигательных и содовых печей путем улучшения качества карбонатного сырья, ликвидации потерь СО2 и подсосов воздуха. [24]
В аммиачно-содовом процессе наиболее сложным и недостаточно изученным является процесс карбонизации аммиачного рассола. [25]
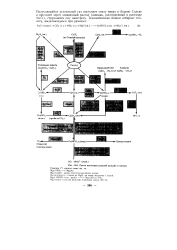 |
Схема некоторых реакций кальция и магния. [26] |
Получающийся углекислый газ поступает снизу вверх в башню Сольве и проходит через аммиачный рассол ( аммиак, растворенный в растворе NaCl), струящийся ему навстречу. [27]
Регулируемыми параметрами, величина которых изменяется при изменении расхода двуокиси углерода, будут расход аммиачного рассола, количество суспензии бикарбоната и расход воды для охлаждения. [28]
Вначале концентрированный рассол, содержащий до 310 г / л NaCl, насыщают аммиаком и получают аммиачный рассол с содержанием до 80 г / л NH3; этот последний затем карбонизуют углекислым газом. [29]
Следует также отметить, что Шлезинг и Ролланд первые перешли от применения углекислого аммония к карбонизации аммиачного рассола. Несмотря на столь значительные усовершенствования аммиачно-сод О Вого процесса, Шлезинга и Ролланда постигла неудача, и они должны были прекратить производство. [30]
Страницы: 1 2 3