Раствор - жидкий аммиак
Cтраница 3
Известны аналогичные, так называемые соли Цинтля, состоящие из катионов щелочных элементов и кластеров металлов в качестве анионов, которые существуют в растворе жидкого аммиака. [31]
Сила кислот и оснований зависит от природы растворителя. В растворе жидкого аммиака, отличающемся сильноосновными свойствами, все кислоты полностью диссоциированы. [32]
 |
Константы ионизации некоторых кислот в СНзСООН при 20 С. [33] |
Таким образом, в среде жидкого аммиака кислотные свойства веществ проявляются сильнее, чем в. Таким образом, в растворе жидкого аммиака различия в силе кислот сглаживаются; это обусловлено большим сродством аммиака к протону. [34]
 |
Константы ионизации некоторых кислот в СНзСООН при 20 С. [35] |
Таким образом, в среде жидкого аммиака кислотные-свойства веществ f проявляются сильнее, чем в воде. Таким образом, в растворе жидкого аммиака различия в силе кислот сглаживаются; это обусловлено большим сродством аммиака к протону. [36]
Таким образом, в среде жидкого аммиака кислотные свойства веществ проявляются сильнее, чем в воде. Таким образом, в растворе жидкого аммиака различия в силе кислот сглаживаются; это обусловлено большим сродством аммиака к протону. [37]
Таким образом, можно констатировать, что в среде жидкого аммиака кислотные свойства веществ проявляются сильнее, чем в воде. Таким образом, в растворе жидкого аммиака различия в силе кислот сглаживаются; это обусловлено большим сродством аммиака к протону. [38]
Жидкий аммиак, обладающий высокой диэлектрической проницаемостью, может использоваться как неводпый растворитель. Как объяснить, что в растворе жидкого аммиака кислоты СН3СООН и НС1О4 диссоциируют нацело, в то время как в водном растворе одна из кислот является слабым электролитом. [39]
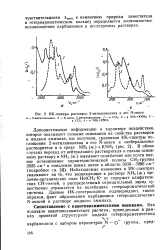 |
ИК-спектры растворен 2-метилхинолина и его М - окиси. а - 2-метилхиколин. б - N-окись 2-метилхинолина. / - в ССЦ. 2 -в NHs KNHj. 3. [40] |
K не содержат алифатических СН-связей, а распределенный отрицательный заряд существенно отражается на колебаниях гетероароматической системы. Данные ИК-спектроскопии подтверждают, таким образом, факт образования карбанионов гетероциклических N-окисей в растворе жидкого аммиака. [41]
Кроме того, свойства веществ под влиянием растворителей настолько меняются, что одно и то же соединение в зависимости от растворителя диссоциирует или как кислота, или как основание. Например, мочевина и бифталат калия являются слабыми основаниями в воде, кислотами в растворе жидкого аммиака и сильными основаниями в среде безводной уксусной кислоты. [42]
Для реакции применяется сииртовый раствор щелочей при нагревании ввиду его способности хорошо растворять галоидопроизводные. Авторы этой книги ( не опубликовано) нашли, что дихлорэтилен и хлорвинил легко образуют ацетилен при действии амида натрия или металлического натрия в растворе жидкого аммиака. [43]
В растворах жидкого аммиака согласно теории сольвосистем все аммонийные соли кислоты, а амиды - основания. Причем последние часто проявляют амфотерность вследствие образования комплексов с НН гв качестве лиганда. Для растворов жидкого аммиака характерен аммонолиз и другие реакции. [44]
В первой стадии в результате переноса одного электрона от лития к енону образуется анион-радикал, который далее протонируется аммиаком до енолят-радикала. Радикал далее восстанавливается литием до литиевого енолята насыщенного кетона. Енолят лития устойчив в растворе жидкого аммиака и протонируется только с помощью более сильных, чем аммиак, протонирующих агентов - хлорида аммония, воды или спирта. [45]
Страницы: 1 2 3 4