Раствор - сильное основание
Cтраница 2
 |
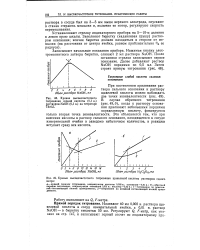
Кривая кондуктометрического титрования смеси ИЫаОН мл хлороводородной и уксусной кислот. [16] |
Определение основано на последовательном взаимодействии с раствором сильного основания NaOH кислот, отличающихся друг от друга степенью ионизации. В первую очередь взаимодействует сильная кислота, что вызывает резкое понижение электрической проводимости раствора вследствие связывания высокоподвижных водородных ионов. При титровании слабой кислоты проводимость обычно возрастает, так как вместо слабого электролита образуется хорошо диссоциирующая соль. И наконец, после точки эквивалентности проводимость резко возрастает благодаря появлению в растворе гидроксиль-ных ионов, обладающих высокой подвижностью. [17]
Гипофосфиты получают кипячением белого фосфора в растворах сильных оснований, их используют в качестве восстановителей при нанесении покрытий из никеля, кобальта и олова на металлы и пластмассы. Фосфорноватистую кислоту получают действием серной кислоты на гипофосфиты, ее используют в производстве полимерных материалов. [18]
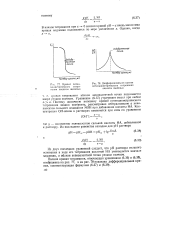 |
Кривая потен-цкометрического титро-пания кислоты щелочью.| Дифференциальная кривая. [19] |
Из двух последних уравнений следует, что рН раствора сильного основания в ходе его титрования кислотой НА уменьшается вначале медленно, а вблизи эквивалентной точки резким скачком. [20]
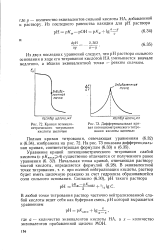 |
Кривая потенцио.| Дифференциальная кривая потенциометрического титрования кислоты щелочью. [21] |
Из двух последних уравнений следует, что рН раствора сильного основания в ходе его титрования кислотой НА уменьшается вначале медленно, а вблизи эквивалентной точки - резким скачком. [22]
Определение всех видов кислотности производят титрованием проб воды растворами сильных оснований. [23]
Кривая кондуктометрического титрования смеси сильной и слабой кислот раствором сильного основания представлена на фиг. [24]
 |
Кривые титрования 0 1 н. растворов. [25] |
Титрование сильных и слабых кислот ( оснований) растворами сильных оснований ( кислот) связано с изменением активностей ионов Н или ОН в растворе. Методы расчета этих величин описаны в книге 2, гл. [26]
Это объясняется тем, что при внесении кислоты в раствор сильного основания, находящегося в сосуде измерительной ячейки в заведомо избыточном количестве, в реакцию вступает сразу вся кислота. [28]
Выделение связанного аммиака осуществимо только при химической обработке воды растворами сильных оснований: гидроксида кальция или натрия. [29]
Триоксид молибдена плохо растворяется в воде, взаимодействует с растворами сильных оснований и аммиака с образованием солей - молибдатов. [30]
Страницы: 1 2 3 4