Раствор - пиридин
Cтраница 2
В каплю раствора пиридина вводят кристалл сулемы. Кристалл покрывается длинными иглами и призмами хлоромеркурата пиридина. Отдельные кристаллы достигают 600 и. [16]
Помещают каплю раствора пиридина на красную лакмусовую бумажку. Затем приливают 0 5 мл этого же раствора к 1 мл раствора хлорного железа. Наблюдается выделение гидроокиси железа. [17]
Ацетилирование в растворе пиридина в присутствии хлорной кислоты протекает медленнее, чем в этилаце-тате. Однако применение пиридина как растворителя имеет и свои преимуществу: в этих условиях определению не мешает присутствие третичных спиртов, соединений с двойными связями и кетонов, за исключением циклопентанона и цнклогексанона. Эти два кетона и альдегиды мешают определению. Параллельное применение двух растворителей позволяет иногда определять раздельно соединения различного строения. Время реакции устанавливается опытом для отдельных спиртов. [18]
Ясно, что раствор пиридина можно использовать для осаждения трудно растворимых гидроокисей, причем концентрацию ОН - - ионов можно регулировать, вводя в систему рассчитанное количество соли пиридиния. [19]
К 1 мл раствора пиридина прибавляют несколько капель 1 % раствора марганцовокислого калия. Обесцвечивания перманганата не наблюдается, что указывает на прочность связей в пиридиновом ядре. [20]
Смешивают 1 мл раствора пиридина с 1 мл перманганата калия и карбоната натрия. Затем нагревают раствор, обесцвечивания не наблюдается. [21]
Смешивают 50 мл раствора пиридина с 5 мл 5 % раствора бензидина. Бутиловый или амиловый спирт. [22]
К 10 мл раствора пиридина добавляют 2 мл раствора бензидингидрохлорида. [23]
К Ю мл 1-процентноговодного раствора пиридина добавляют одну каплю 10-процентного раствора сульфата меди и после перемешивания 1 каплю 20-процентного раствора роданида калия или аммония; появляется ] характерный зеленый осадок. [24]
Ацетилирование полиоксифлавонов в растворе пиридина при комнатной температуре не затрагивает оксигруппы в положении GS вследствие наличия водородной связи, а если реакцию проводить при 100, то ацетилирование можно осуществить. [25]
Тетрафенилборкалий реагирует в растворе пиридина с медьацетоуксус-ным эфиром с образованием пиридината тетрафенилбормеди, CuB ( CeH5) 4 - 4C6H5N, [149] - светло-желтого порошка, из которого при осторожном подкислении выделяется тетрафенилбормедь - - малоустойчивое бесцветное вещество. Пиридинат тетратолилбормеди, полученный аналогичным образом, отличается неустойчивостью. Тетратолилбормедь, как таковую, не удалось получить вышеуказанным способом; при попытке отщепить пиридин ( разбавленной H3SO4) были выделены дитолил и металлическая медь. [26]
К 0 5 мл раствора пиридина прибавляют 1 - 2 мл насыщенного раствора пикриновой кислоты. Получаются желтые игольчатые кристаллы трудно растворимого пикрата пиридина. [27]
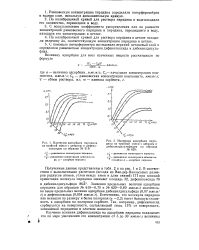 |
Изотермы адсорбции пиридина.| Изотермы адсорбции пиридина из тройной смеси с цетаном и дибензилдисульфидом на образце № 620. [28] |
По калибровочной кривой для раствора пиридина в воде находили его количество, перешедшее в воду. [29]
Удобно вести ацилирование в растворе пиридина, как алифатическими, так и ароматическими хлорангидридами и ангидридами кислот. В этих условиях ацилирование может проходить количественно. [30]
Страницы: 1 2 3 4