Раствор - продукт - реакция
Cтраница 3
Защищенным анодом автор называет горизонтально расположенный электрод, оправленный в изолятор. Поверхность такого анода покрыта раствором продукта реакции ( Прим. [32]
 |
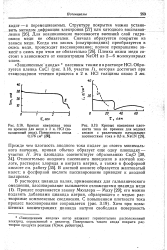
Температурная зависимость выхода хлористого этила и полимеров этилена при гидрохлорировании этилена в присутствии хлористого алюминия. [33] |
Синтез хлористого этила гидрохлорированием этилена осуществляют по непрерывной схеме путем барботирования этилена и хлористого водорода через жидкий хлористый этил, содержащий катализатор. Исходные газы реагируют в растворе продукта реакции, и в этом отношении данный процесс аналогичен синтезу дихлорэтана или тетрахлорэтана из соответствующих углеводородов и хлора. [34]
По мере накопления в растворе продуктов реакции перманганат начнет обесцвечиваться значительно быст-рее. Если розоватая окраска раствора исчезнет через более продолжительное время, то на это не следует обращать внимания, и титрование можно считать законченным. [35]
В свежеприготовленном растворе продолжительность травления устанавливают по нижнему ее пределу. По мере накопления в растворе продуктов реакции и Сг3 ее увеличивают. После этого процесс травления значительно замедляется, раствор становится вязким и его регенерируют или заменяют. [36]
Первые 1 - 2 мл КМпО4 приливают медленно, по каплям, добавляя каждую каплю только после обесцвечивания предыдущей и сильно перемешивая раствор. По мере накопления в растворе продуктов реакции обесцвечивание перманганата происходит значительно быстрее, так как образующийся ион Мп2 - катализатор реакции. [37]
Растворяют 0 5 г первичного амина и 1 5 г л-нитробензилхлорида в 10 - 20 мл спирта, прибавляют раствор 0 4 г безводной соды в 5 - 10 мл воды и кипятят 1 ч в колбе, соединенной с обратным холодильником. Прибавляют воду для выделения из раствора продукта реакции, перекристаллизовывают его из воды и определяют температуру плавления. [38]
Растворяют 0 5 г первичного амина и 1 5 г n - нитробензилхлорида в 10 - 20 мл спирта, прибавляют раствор 0 4 г безводной соды в 5 - 10 мл воды и кипятят 1 ч в колбе, соединенной с обратным холодильником. Прибавляют воду для выделения из раствора продукта реакции, перекристаллизовывают его из воды и определяют температуру плавления. [39]
 |
Устройство для химико-динамического полирования подложек полупроводников типа Конус. [40] |
Объем травителя во избежание накопления в растворе продуктов реакции травления и для поддержания изотермических условий и стабилизации гидродинамических потоков должен составлять 10 - 15 см3 / см2 поверхности пластины полупроводника. Скорость циркуляции травителя подбирают экспериментально с учетом геометрии сосуда с раствором. [41]
Уксусная кислота в этих условиях образует вшшл-и этилиденацетаты, а спирты-ацетали; но все эти вещества в присутствии водных кислот гидролизуются в ацетальдегид. Повышение растворимости ацетилена и более длительное пребывание в растворе продуктов реакции имеет свою отрицательную сторону-повышенное образование продуктов конденсации. Поэтому сомнительно, смогут ли преимущества от добавления органических растворителей к каталитическому раствору компенсировать увеличивающиеся трудности выделения и очистки ацетальдегида. [42]
Все три вещества обладают асимметрическим атомом углерода и являются оптически активными. Водный раствор тростникового сахара вращает плоскость поляризации проходящего света вправо, раствор продуктов реакции - влево. По мере течения реакции правое вращение сменяется левым. [43]
По окончании этой реакции раствор переходит в третью зону, имеющую самую высокую концентрацию компонента в газовой фазе. Скорость процесса в этой зоне определяется скоростью физической абсорбции компонента в раствор продуктов реакции, аналогично абсорбции труднорастворимого газа. [44]
При этом гидроксид натрия прореагировал полностью и образовался 16 55 % - ный раствор продукта реакции. [45]
Страницы: 1 2 3 4