Раствор - сера
Cтраница 2
Удельные веса растворов серы в сероуглероде ( отнесенные к воде при 4), соответствующие весовым количествам серы, которые содержатся в 100 вес. [16]
Здесь принимается, что раствор серы в железе является разбавленным, поэтому ее концентрация [ S ] пропорциональна активности. Активность железа в металлической фазе равна единице, так как концентрации всех примесей в рассматриваемом случае очень малы. [17]
Одним из ядов является раствор серы ( 1 г) в хинолине ( 6 г), который получают нагреванием смеси этих веществ в течение 5 ч и последующим разбавлением жидкости до объема 70 мл очищенным ксилолом. Ксилол очищают кипячением с натрием ( 0 5 г натрия на 250 мл ксилола) в течение 25 ч с последующей перегонкой. Хранят ксилол над натрием. Во многих других каталитических реакциях гидрирования, когда желательно осуществить лишь частичное гидрирование, к катализаторам прибавляют яды. Например, при гидрировании ацетилена до этилена над палладием на кизельгуре избирательности действия катализатора достигают прибавлением ртути. Для той же цели частичного гидрирования тройной связи применяют палладиевые катализаторы на некоторых носителях, отравленные ацетатом свинца ( по Линдляру, см. стр. [18]
Установившееся равновесие между подачей раствора серы в сероуглероде из куба колонны в сероотделитель и работой холодильника фиксируется положением рукоятки крана и при дальнейших пусках кран сразу открывается на такую же величину. Как правило, при первоначальном пуске дистилляционной системы включение сероотделения следует производить через 2 - 3 ч после начала работы дистилляционной колонны. Сильное запаздывание, особенно при высоком содержании сухого остатка в сыр це, может привести к положению, когда выводная труба, опущен ная на дно колонны, окажется забитой серой. [19]
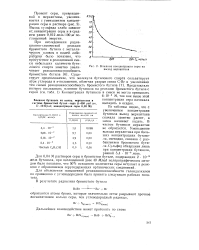 |
Влияние концентрации серы на выход меркаптана. [20] |
Для 0 04 М растворов серы в бромистом бутиле, содержащих 2 10 - 3 Мбль бутанола, при поглощенной дозе 40 Мрад полярографическим методом было показано, что 50 % исходного количества серы вступает в реакцию с образованием серусодержащих органических соединений. [21]
Дефектные решетки образуются в растворах серы и селена в соединениях CaS и FeS, железа в CoFe и FeTe, сурьмы в NiSb в сплавах Ni - А1, Со - А1, тантала в ТаС, титана в TiC, ниобия в NbC, циркония в ZrC, ванадия в VC. Фазы - твердые растворы вычитания-широко встречаются в сверхтвердых сплавах. [22]
При встряхивании металлической ртути с сероуглеродным раствором серы получается HgS, в котором сера открывается также известными методами. [23]
При облучении у-лучами ( 60Со) раствора серы в толуоле процесс димеризации бензильных радикалов с образованием дифе-нилэтана не наблюдается; в основном получаются сероводород и бензилмеркаптан. [24]
Так, измерение повышения точки кипения раствора серы в сероуглероде ясно показывает, что сера в этом растворе существует в виде молекул, состоящих из 8 атомов. [25]
 |
Конструкции эксплуатационных скважин для подземной. [26] |
Для разделения подаваемого рабочего агента от поднимаемого раствора серы в нижней части раствороподъемной трубы на расстоянии 100 - 500 мм от ее нижнего конца предусматривается установка кольцевого пакера, вторая часть которого устанавливается на эксплуатационной трубе, предназначенной для подачи теплоносителя. [27]
По окончании процесса экстракции в угле остается раствор серы в перхлорэтилене, количество раствора определяется адсорбционной способностью угля по перхлорэтилену при температуре экстракции. Если сразу провести десорбцию перхлорэтилена из угля ( температура десорбирующего пара 130 - 140 С), то на угле останется элементарная сера, так как температура ее испарения намного превышает температуру кипения перхлорэтилена. Для остаточного достижения содержания серы в угле дост 1 % ( масс.), необходимо проводить повторную экстракцию. [28]
Золь серы был получен добавлением 5 см3 раствора серы в спирте к 10 см3 дистиллированной воды. Каким методом получен золь. Чем объясняется, что в проходящем свете золь имеет красновато-оранжевый оттенок, а в отраженном - голубоватый. [29]
Наибольшее значение молярного коэффициента погашения наблюдается для растворов серы в изопропиловом спирте и четыреххлористом углероде ( 1400 и 910 соответственно); однако область спектра, где расположен максимум оптической плотности для растворов серы в изопропиловом спирте ( 222 ммк), находится вблизи от границы пропускания оптики спектрального прибора ( СФ-4), что приводит к снижению точности и чувствительности определения, поэтому мы предпочли использовать в качестве экстрагента четыреххлористый углерод. [30]
Страницы: 1 2 3 4