Раствор - смесь - соль
Cтраница 1
Раствор смеси солей имеет осмотическое давление, равное сумме осмотических давлений растворенных компонентов. Следует отметить, что увеличение этих давлений в дисперсных системах вследствие наличия дисперсной фазы мало из-за влияния концентрации. Его величина зависит от природы и размера частиц. Осмотическое давление растворов высокомолекулярных веществ возрастает быстрее, чем увеличивается концентрация. Это объясняется тем, что возрастает число сегментов, на которые условно можно разделить гибкую макромолекулу. [1]
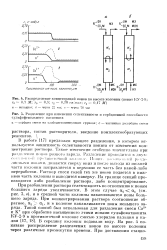
Раствор смеси солей тех же ионов подается в нижнюю часть колонны и выводится наверху. На границе секций производится либо разбавление раствора, либо концентрирование. При разбавлении раствора селективность по отношению к ионам большего заряда увеличивается. В этом случае 2 cq ( см. рис. 3, в), и в средней части колонны накапливаются ионы большего заряда. При концентрировании раствора соотношение обратное, а2 а15 и в колонне накапливаются ионы меньшего заряда. [3]
Раствор смеси солей был предложен Хадсоном и содержал четыре иона, которые находятся в большом количестве в обыкновенной атмосфере. [4]
Хроматографируя растворы смеси солей тех же катионов в различных сочетаниях, а также смесь всех катионов при одновременном их присутствии в растворе, получают первичные, промытые и проявленные хроматограммы. [5]
К раствору смеси солей железа и алюминия в стакане для осаждения добавляют 5 мл НС1 ( пл. Окисление железа проводят, как описано в предыдущей методике. Затем, ополаскивая внутренние стенки стакана и часовое стекло дистиллированной водой, доводят объем раствора до 130 - 150 мл. Осаждение водных оксидов проводят, добавляя в теплый раствор при перемешивании по каплям из бюретки разбавленный водный 10 % - ный раствор аммиака до изменения окраски индикатора метилового красного из красной в желтую. [6]
При упаривании раствора смеси солей обнаруживается высаливающее действие металлилсульфоната натрия, а при охлаждении упаренного раствора - высаливающее действие хлористого натрия. [7]
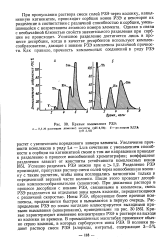 |
Кривые вымывания РЗЭ. [8] |
При пропускании раствора смеси солей РЗЭ через колонку, наполненную катионитом, происходят сорбция ионов РЗЭ и некоторое их разделение в соответствии с различной способностью к сорбции, уменьшающейся с возрастанием атомного номера элемента. Однако в связи с необычайной близостью свойств значительного разделения при сорбции не происходит. Успешное разделение достигается лишь в процессе десорбции, когда в качестве десорбентов используют комплек-сообразователи, дающие с ионами РЗЭ комплексы различной прочности. [9]
А) Обработывают раствор смеси солей избытком твердой сернокалиевой соли. Этот обычный способ деления оказывается, однако, по исследованиям Мариньяка, настолько недостаточным, что в растворимой части остается много Di и других металлов, которые, будучи в смеси, растворяются, а в отдельности нерастворимы. Так, эрбий и тербий находятся и в растворе и в осадке. Тем не менее укажем, что к растворимым относятся: Be, Y, Ег, Yb j, а к нерастворимым: Sc, Ce, La, Di, Th. [10]
Упаренные ( насыщенные) растворы смеси солей подвергаются электролизу, а затем могут использоваться вместо применяемых в настоящее время соды и извести для умягчения сточных вод и для хлорирования оборотных вод, а получаемый сульфат натрия направляется к потребителю. [11]
Следовательно, при электролизе раствора смеси солей водород выделяется только за счет электролиза раствора Ва ( МОз) г, кислород - за счет обеих солей. Это значит, что количество грамм-эквивалентов азотнокислого бария, а значит и его молей, было в два раза больше, чем нитрата меди. [12]
 |
Разделение соли и спирта по методу исключения ионов. [13] |
При внесении в колонку раствора смеси соли и органического соединения, не электролитной природы, органическое соединение в принципе, должно распределиться равномерно по всему объему, при условии, что оно не адсорбируется смолой. [14]
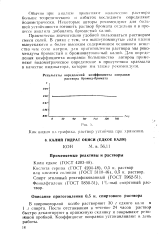 |
Как видно из графика, раствор устойчив при хранении. [15] |
Страницы: 1 2 3 4