Раствор - смесь - соль
Cтраница 3
В табл. 2 на результатах нашего анализа и измерений электропроводности раствора смеси солей, водной вытяжки почвы и грунтовой воды показано несоответствие между изменениями коэффициентов Долгова и Житковой и электропроводности с разведением. [31]
На рис. Х-13 приведена диаграмма для определения плотности и температуры кипения растворов смеси солей CO ( NH2) 2 NH4H2PO4 KC1 при соотношении N: Р2О5: К2О1: 1: 1 в зависимости от концентрации и давления. [32]
Какие вещества и в какой последовательное будут выделяться на электродах при электролизе раствора смеси солей; хлорида магния, сульфата никеля ( II), нитрата цинка. [33]
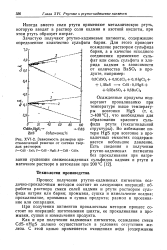 |
Зависимость размеров кристаллической решетки от состава твердых растворов. I-CdS ZnS. 2 - CdS HgS. 3 - CdS CdSe. [34] |
Процесс получения ртутно-кадмиевых пигментов оса-дочно-прокалочным методом состоит из следующих операций: обработка раствора смеси солей кадмия и ртути раствором сульфида натрия или бария; промывка, сушка и измельчение осадка; прокаливание, промывка и сушка продукта; размол и просеивание или сепарация. [35]
Реакция образования берлинской лазури основана на свойстве синильной кислоты вступать во взаимодействие с раствором смеси солей, закиси и окиси железа. [36]
Метод распылительной сушки растворов заключается в быстрой сушке мелко распыленного в сушилках соответствующей конструкции раствора смеси солей. В результате получают тонкодисперсный порошок высокой активности. Температура сушки должна соответствовать температуре начала спекания веществ, входящих в состав высушенной и прокаленной массы. [37]
Хантер [28] предложил более простой вариант метода быстрых, обменных реакций, в котором используются первоначально растворы смеси солей анализируемых кислот и этилсульфата калия. [38]
Таблетки после сушки ( при 70 - 320 С) прокаливают в токе воздуха 4 - 48 ч, затем обрабатывают раствором смеси солей СоС12 и NH4C1 концентрацией 9 и 2 г / л в течение 24 ч при 20 С. [39]
Способ разделения и ы - дикарбоновых кислот, содержащих более 6 атомов углерода, из смеси, выпадающей при их получении, отличающийся тем, что из растворов смеси солей отдельные дикарбоновые кислоты выпадают одна за другой при ступенчатом регулировании концентрации водородных ионов. [40]
В растворе К2 [ PtClJ концентрации частиц, образующихся при ступенчатой диссоциации иона [ PtQ4 ] 2 -, крайне незначительны, в то время как в разбавленном растворе К2 [ CuClJ практически отсутствуют комплексные ионы [ CuClJ2 и по характеру образующихся частиц диссоциация этой соли ничем не отличается от диссоциации в растворе смеси солей К. [41]
В растворе K2 [ PtCl4 ] концентрация частиц, образующихся при ступенчатой диссоциации иона [ PtCl4 ] 2, крайне незначительна, в то время как в разбавленном растворе К2 [ СиС14 ] практически отсутствуют комплексные ионы [ СиС14 ] 2 - и по характеру образующихся частиц диссоциация этой соли ничем не отличается от диссоциации в растворе смеси солей КС. [42]
Из раствора смеси солей путем добавления углекислого аммония образуются углекислые соли. После промывки, фильтрации и сушки осадок прокаливают до полного разложения гидратов или карбонатов. Прокаленный осадок вновь измельчают, порошок брикетируют и обжигают при температуре, при которой завершается шпинелеобразование. Обожженные брикеты дробят, размалывают в порошок, и он поступает на изготовление изделий. Синтезированная по одному из описанных способов шпинель является исходным полупродуктом для изготовления изделий той или иной формы. [43]
С помощью ионообменной хроматографии была успешно решена задача получения чистейших препаратов РЗЭ. При пропускании раствора смеси солей РЗЭ через колонку, наполненную катионитом, происходит некоторое разделение РЗЭ благодаря различной способности их к ионообменной адсорбции. Последняя уменьшается с возрастанием атомного номера элемента. Однако в связи с необычайной близостью свойств РЗЭ достичь эффективного разделения таким путем не удается. Успех может быть только при применении в качестве десорбентов комплексообразующих агентов, дающих с РЗЭ комплексы различной устойчивости. Благодаря тому что устойчивость комплексных соединений в ряду редкоземельных элементов, как правило, растет с увеличением порядкового номера, а сорбируемость на катионите падает в том же направлении, эффект разделения увеличивается. [44]
Наиболее широко в технологии редких металлов ионный [ Iобмен применяют для разделения лантаноидов. При пропускании раствора смеси солей РЗЭ через колонку, наполненную катионитом, происходит частичное разделение благодаря различной способности к ионному обмену. Ионообменное разделение основано на том, что постепенное уменьшение радиуса иона ( и соответствующее понижение основности) приводит к постепенному упрочнению связи с гидратной оболочкой. Поскольку в основе прочности связывания катионов с анионными группами ионообмен-ников лежит, по-видимому, электростатическое притяжение гидратированного катиона к отрицательной группировке, то оказывается: чем больше радиус гидратированного noffa, тем менее прочно он связывается. [45]
Страницы: 1 2 3 4