Раствор - соль - кадмий
Cтраница 3
Последние улавливают в раствор щелочи и титруют раствором соли кадмия или ртути в присутствии дитизона. [31]
Затем в электролизер по каплям добавляют стандартный, раствор соли кадмия ( содержащий 1 мг / мл) до тех пор, пока волна кадмия не возрастет примерно вдвое. Не изменяя чувствительности гальванометра, измеряют высоты волн и рассчитывают содержание кадмия в электролите. [32]
При действии тиоцианатов щелочных металлов или аммония на растворы солей кадмия в присутствии пиридина осаждается соединение [ Cd ( C5H5N) 2 ] ( SCN) 2 белого цвета, растворимое в избытке пиридина. [33]
 |
Скорость пассивирования серебра ( 0 2 н. раствор AgN03. [34] |
Таким образом, не только платиновый электрод в растворе соли кадмия или серебра является инертным, пока на нем не возникнут первые кристаллы ( один или несколько), но также инертен и серебряный электрод в растворе соли серебра. [35]
Гидроокись кадмия Cd ( OH) 2 выделяется из растворов солей кадмия при действии едких щелочей в виде белого студенистого осадка, практически нерастворимого в избытке ре агента, но легко растворяющегося в кислотах, цианидах и аммиаке. [36]
Этим объясняется тот факт, что избыток аммиака с растворами солей кадмия, как и с солями меди ( П), не дает осадка. Кроме того, CdCl2 образует и неионизируемый аммин Сс1С12 ( МН3) 2, который, несмотря на аналогию этой эмпирической формулы с формулой одного соединения цинка ( стр. [37]
Согласно Денхаму и Маррису [5] и Кентен [6] гидролиз в растворах солей кадмия несколько больше, чем в растворах солей цинка, в то время как по данным Чупра [7] - несколько меньше. [38]
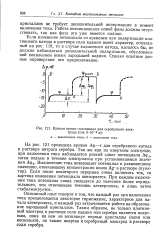 |
Кривая время-потенциал для серебряного электрода ( ток 3 - 10-в а. [39] |
Если изменение потенциала со временем при поляризации платинового катода в растворе соли кадмия имеет характер, показанный на рис. 118, то в случае кадмиевого катода, казалось бы, не должно наблюдаться дополнительной поляризации, обусловленной появлением новых зародышей кадмия. Однако опытные данные опровергают это предположение. [40]
Согласно Денхаму и Маррису [5] и Кентен [6] гидролиз в растворах солей кадмия несколько больше, чем в растворах солей цинка, в то время как по данным Чупра [7] - нескол ко меньше. [41]
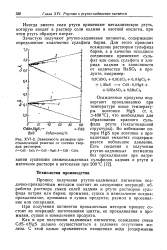 |
Зависимость размеров кристаллической решетки от состава твердых растворов. I-CdS ZnS. 2 - CdS HgS. 3 - CdS CdSe. [42] |
Иногда вместо соли ртути применяют металлическую ртуть, которую вводят в раствор соли кадмия и азотной кислоты, при этом ртуть образует нитрат. [43]
На фильтровальную бумагу помещают каплю раствора KBiJ4, а затем каплю раствора соли кадмия. [44]
Исследованиями ряда авторов [ 7-и ] было показано, что при взаимодействии растворов солей кадмия ( нитраты, сульфаты, хлориды) с аммиаком сначала идет обменная реакция с выделением гидроокисных осадков различного состава ( основные соли и основные аммиакаты) в зависимости от концентрации исходных продуктов и их молекулярных отношений. Последующее добавление аммиака приводит к растворению осадков и образованию растворимых комплексных аммиакатов. В системе CdS04 - NH3 - Н20 образование гидроокиси кадмия возможно лишь в очень разбавленных растворах - 0.005 мол. [45]
Страницы: 1 2 3 4