Раствор - соль - хром
Cтраница 3
Затем приливают по каплям раствор соли хрома ( II) до исчезновения окраски индикатора и еще небольшой избыток. [31]
Почему при введении в растворы солей хрома ( III) сульфид - или карбонат-ионов выпадает осадок одинакового состава. [32]
Затем приливают по каплям раствор соли хрома ( II) до исчезновения окраски индикатора и его небольшой избыток. [33]
К 0 5 мл раствора соли хрома ( III) добавляют 0 5 мл раствора кобальтового катализатора и нагревают до кипения. В кипящий раствор вводят твердый персульфат аммония ( примерно 0 1 г) и кипятят 20 - 30 с. В присутствии хрома раствор окрашивается в желтый цвет. [34]
К 0 5 мл раствора соли хрома ( III) добавляют раствор КМпО4 до появления неисчезающей при кипячении розовой окраски. Прибавляют 2 - 3 капли раствора соли марганца ( II), еще раз доводят до кипения и фильтруют. [35]
С этой целью к раствору соли хрома приливают щелочь; получающийся осадок Сг ( ОН) 3 растворяют в избытке щелочи, после чего прибавляют перекись водорода НЮ. [36]
С этой целью к раствору соли хрома приливают щелочь; получающийся осадок Сг ( ОН) 3 растворяют в избытке щелочи, после чего прибавляют перекись водорода Н2О2 и нагревают до тех пор, пока раствор из зеленого не станет желтым. [37]
К 2 - 3 каплям раствора соли хрома ( III) прибавляют 4 - 5 капель 2 и. NaOH, 2 - 3 капли 3 % - ного раствора перекиси водорода и нагревают несколько минут до тех пор, пока зеленая окраска раствора не перейдет в желтую. [38]
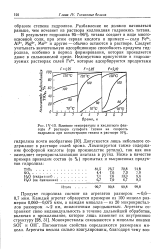 |
Влияние температуры и кислотного фактора F раствора сульфата титана на скорость гидролиза при концентрации титана в растворе 10 %. [39] |
Допускается лишь небольшое содержание в растворе солей хрома. Лимитируется также содержание фосфорной кислоты ( при производстве рутила), так как она замедляет перекристаллизацию анатаза в рутил. [40]
Фосфат хрома СгРО4 образуется при действии Na2HPO4 на раствор соли хрома. Образующийся осадок СгРО4 серо-зеленого ( иногда фиолетового цвета) растворим в кислотах ( минеральной, уксусной) и в щелочах. [41]
В результате взаимодействия избытка раствора гидроксида натрия на раствор соли хрома ( III) образуется раствор хромита натрия. [42]
В фарфоровую чашку помещают 18 - 20 капель раствора соли хрома и выпаривают досуха. Платиновую проволоку прокаливают в пламени горелки, раскаленной петлей захватывают кристаллы тетрабората, прокаливают их в пламени горелки, охлаждают полученный перл, захватывают перлом сухую пробу из чашки, снова прокаливают и после охлаждения наблюдают образование перла, окрашенного в изумрудно-зеленый цвет. [43]
За последнее время предложено много новых вариантов приготовления растворов трехвалентных солей хрома, производятся испытания. В смысле простоты электролиза некоторый интерес приобретает хлоридный процесс; его надо организовать так, чтобы использовать для выщелачивания руды ( или феррохрома. [44]
При потенциометрическом титровании перрената калия в солянокислой среде раствором соли хрома ( II) потенциал платинового анодно поляризованного электрода устанавливается быстро [80]; в точке эквивалентности наблюдается отчетливый скачок потенциала. [45]
Страницы: 1 2 3 4