Гликолевой раствор
Cтраница 1
Гликолевые растворы, имеющие кислую реакцию в результате автоокисления или введения уксусной кислоты, во всех случаях более агрессивны, чем нейтральные растворы. [1]
Гликолевые растворы в щелочной среде вызывают лишь сравнительно медленную коррозию. [2]
В гликолевых растворах отсутствует характерный для аодных растворов горб на С - ф-кривых. Однако С-ф-кривые кислородсодержащих анионов характеризуются некоторой задержкой в области потенциалов, соответствующих положительным зарядам поверхности. [3]
При наличии в составе гликолевых растворов минеральных солей вязкость системы увеличивается. Прибавление в систему воды снижает вязкость. [4]
Определение основано на титровании смеси NaOH и СНзСООКа стандартным гликолевым раствором НС1О4 с двумя индикаторами - фенолфталеином и метиловым оранжевым, применяемыми последовательно. [5]
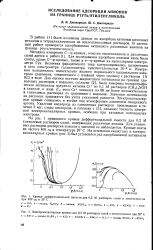
На рис. 1 приводятся кривые дифференциальной емкости для 0 2 М гликолевых растворов солей, содержащих различные анионы. Для указанных растворов дисперсия емкости с частотой не наблюдается. Кривые сняты на частоте 400 щ и температуре 20 С. [7]
Несмотря на плоскую ориентацию молекул гликоля на поверхности ртути [4], сдвиг ТНЗ в положительную сторону в гликолевых растворах KF по сравнению с водными является ощутимой величиной и обусловлен ориентацией С - О-связи кислородом в сторону раствора. [8]
Водно-спиртовые и водно-гликолевые растворы ( смеси из спирта, пропиленгликоля, глицерина, воды), а также спиртовые и гликолевые растворы очень часто применяются для улучшения растворимости действующих веществ, и, соответственно, дают возможность применения более высокой концентрации вещества. Эти растворы оказывают подсушивающий эффект, в некоторых случаях смягчающее действие. Растворители и их смеси в данных составах могут также применяться для повышения стабильности некоторых веществ. [9]
Результаты наших исследований по адсорбции катионов 11 ] и анионов из гликолевых растврров подтверждают мнение авторов [11], что из растворителей с низким значением D адсорбционная активность катионов выше, а анионов ниже, чем из воды. Следует отметить, что из гликолевых растворов анион С1 - по сравнению с другими анионами проявляет значительную адсорбционную активность, чем из водных растворов. Следует также отметить, что экспериментальная электрокапиллярная кривая в гликолевых растворах для KJ ( рис. 2, кривая 6) незначительно, но все же систематически проходит ниже экспериментальной кривой 1 для фонового электролита K. [10]
В работах [7, 8 ] высказано предположение, что анионы С1О - и NO - выжимаются из объема на поверхности ртути, и между ними и поверхностью ртути остается прослойка молекул воды. Низкое значение а в ТНЗ в гликолевых растворах по сравнению с водными ( рис. 2), снижение емкости при введении в водный раствор примесей гликоля [1, 4], а также величины работ адгезии гликоля на ртути ( 150 3 эрг / см) и воды на ртути ( 130 6 эрг / см) [9] однозначно показывают высокую адсорбционную активность молекул гликоля на поверхности ртути по сравнению с молекулами воды. [11]
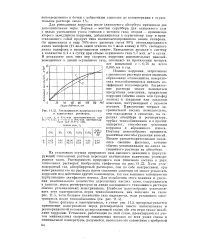 |
Растворимость природного газа в гликолевых растворах. [12] |
На установках осушки природного газа высокого давления в циркулирующий гликолевый раствор переходит значительное количество углеводородных газов. Растворимость природного газа типичного состава в двух гликолевых растворах изображена графически на рис. 11.22. Хотя углеводородный газ, абсорбируемый раствором, сам по себе неагрессивен, при выветривании его из раствора путем снижения давления он может усиливать коррозию под действием других компонентов, так как вызывает интенсивную турбулизацию двухфазного потока. Для ослабления этого влияния и удаления максимального количества агрессивных кислых газов, содержащихся в гликоле, перед регенератором на линии насыщенного гликолевого раствора обычно устанавливают выветриватель. [13]
В [1 ] было показано, что в гликолевых растворах действительно наблюдается резкое увеличение адсорбируемости катионов. По результатам настоящей работы видно, что поверхностная активность анионов в гликолевых растворах, по сравнению с водными, резко уменьшается. Из сопоставления данных настоящей работы с данными работ, проведенных для других неводных растворителей, видно, что величина поверхностной активности анионов мало зависит от величины макроскопической диэлектрической постоянной растворителя ( D) и в основном определяется энергией их сольватации. Из растворов диметилформамида, ди-метилсульфоксида и сульфолана, наоборот, наблюдается сильная специфическая адсорбция анионов [3, 9], так как в этих апротонных растворителях они слабо сольватированы. D независимо от типа растворителя. Например, в гликолевых ( D37 7) и диметилформамидных ( D36 7) [3] растворах ряд адсорбционной активности анионов почти совпадает, несмотря на то, что гликоль является протонным, а диметилфор-мамид - апротонным растворителем. [14]
Смесь NaOH и CH3COONa помещают в мерную колбу вместимостью 50 мл и доводят до метки смешанным растворителем ( этиленгликоль изопропиловый спирт) с помощью капилляра с каучуковым наконечником. В колбу для титрования отбирают аликвоту ( 5 00 мл) полученного раствора, добавляют 20 мл гликолевой смеси и несколько капель фенолфталеина. Анализируемую смесь титруют стандартным 0, 1М гликолевым раствором НС1О4 до исчезновения розовой окраски. К бесцветному раствору добавляют 1 каплю метилового оранжевого и продолжают титрование до перехода окраски из желтой в оранжевую. [15]
Страницы: 1 2