Цинкатной раствор
Cтраница 3
В последнее время широко применяются сложные так называемые модифицированные цинкатные растворы. Сложные цинкатные растворы содержат дополнительные компоненты - хлорное железо и сегнетову соль и имеют ряд преимуществ перед обычными цинкатными растворами. [31]
Значительное влияние на работу щелочно-цинковых элементов оказывает большая склонность цинкатных растворов к расслаиванию, когда более тяжелый цинкат скапливается внизу элементного сосуда, вытесняя в верхние его зоны более легкую щелочь. Это свойство используется в практике применением для элементов с монолитными анодами высоких сосудов и установкой блока элемента в их верхней части. Элементный блок при этом находится в растворе с концентрацией цинката ниже средней, что позволяет более полно использовать щелочь электролита. Расслоение электролита вызывает некоторую неравноценность работы цинкового анода по высоте. [32]
После тщательной промывки в воде детали вновь обрабатывают в цинкатном растворе. [33]
При цинковании в кислых электролитах подготовку производят также в цинкатном растворе, как и перед никелированием. Для цинкования алюминия и его сплавов пригодны обычные сернокислые электролиты. [34]
Из рисунка видно, что ири осаждении цинка в щелочных цинкатных растворах поляризация катода плавно растет во времени аналогично кривым, полученным из цианистых растворов. [36]
Наибольшее применение находят способы хромирования с предварительной обработкой деталей в цинкатных растворах, цель которой - создание очень тонкой и равномерной защитной пленки на поверхности обрабатываемых деталей перед хромированием. [37]
Приведенные данные свидетельствуют о возможности получения плотных осадков цинка при электролизе цинкатных растворов при таких катодных плотностях тока в импульсах, которые в десятки раз превышают предельные значения тока. [38]
Исходя из этих представлений, мы44 считаем, что при электролизе цинкатных растворов на катоде наряду с комплексными ионами разряжаются нейтральные частицы гидроокиси цинка. Возникновение губчатых осадков на отдельных точках катода связано с недостатком частиц Zn ( OH) a около таких точек. При общей значительной концентрации цинка в электролите губка на катоде все же образуется, когда гидроокись цинка восстанавливается на предельном токе. Медленность образования новых частиц гидроокиси цинка при гидролизе приводит к тому, что на образование губки влияет объемная плотность тока; когда последняя велика, губка образуется скорее. [39]
Обнаружено, что факторы, оказывающие значительное влияние на процесс старения пересыщенных цинкатных растворов, сильно воздействуют и на работу щелочноцинковых элементов. С повышением температуры отмечается более раннее выпадение осадка в элементах; при более высоких температурах элементы раньше выходят из строя вследствие наблюдающейся пассивации цинкового электрода. [40]
В формуле вместо активностей подставлены концентрации, так как значения активностей для цинкатных растворов не известны. В солевых растворах в начале при разряде образуется окись или гидроокись цинка, которая затем либо переходит в электролит в виде коллоидных частиц ZnO [ Zn ( OH) 2 ], либо образует гетаэролит Zn ( MnOO) 2, либо дает комплексные соединения с NH4C1 электролита. Потенциал Zn в хлоридных растворах равен - 0 7н - 0 8 в. Применение магниевого электрода представляет интерес из-за его более отрицательного ( по сравнению с цинком) потенциала и малого эквивалентного веса. [41]
В формуле вместо активностей подставлены концентрации, так как значения активностей для цинкатных растворов не известны. В солевых растворах в начале при разряде образуется окись или гидроокись цинка, которая затем либо переходит в электролит в виде коллоидных частиц ZnO [ Zn ( OH) 2 ], либо образует гетаэролит Zn ( MnOO) 2, либо дает комплексные соединения с NH4C1 электролита. Применение магниевого электрода представляет интерес из-за его более отрицательного ( по сравнению с цинком) потенциала и малого эквивалентного веса. [42]
Для цинкатной обработки алюминиевых сплавов, содержащих значительное количество меди, рекомендуется в цинкатном растворе заменять окись цинка эквивалентным количеством сульфата цинка. [43]
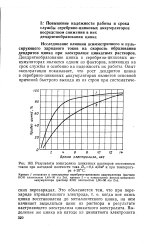 |
Результаты электролиза цинкатных растворов постоянным током при катодной плотности тока DK0 4 а / дм2 и при температуре 20 С. [44] |
Исследование влияния асимметричного и пульсирующего зарядного токов на скорость образования дендритов цинка при электролизе цинкатных растворов. [45]
Страницы: 1 2 3 4