Метастабильный раствор
Cтраница 1
Метастабильные растворы по сравнению с лабильными растворами того же вещества всегда являются менее концентрированными. Таким образом, при увеличении концентрации метаста-бильный раствор переходит в лабильное состояние. Концентрация, при которой совершается переход, называется границей метастабильности. [1]
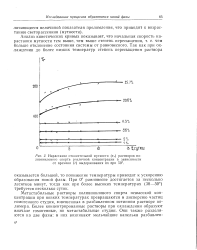 |
Нарастание относительной мутности ( тг растворов поливинилового спирта различной концентрации в зависимости от времени ( t выдерживания их при 50. [2] |
Метастабильные растворы поливинилового спирта невысокой концентрации при низких температурах превращаются в дисперсию частиц гомогенного студня, взвешенных в разбавленном истинном растворе полимера. Более концентрированные растворы при охлаждении образуют вначале гомогенные, но метастабильные студни. [3]
 |
Старение эквивязких в начальный момент времени растворов сополимера и пол. И-ж-фениленизофталамида различного молекулярного веса. Цифры на кривых - Т1УД полимера. [4] |
Получаемые метастабильные растворы в ряде случаев имеют достаточно продолжительное время жизни, благодаря чему находят практическое применение. [5]
В метастабильных растворах, претерпевающих расслоение, полимерная фаза может выделяться и на частицах наполнителя. В этом случае в контактных зонах образуются полимерные про -, слойки, играющие роль склеек и значительно повышающие прочность контактов между частицами. Эффект повышения прочности контактов при выделении в контактных зонах полимерной фазы не зависит от природы поверхности частиц. [6]
Так как метастабильный раствор характеризуется кристаллизационным и карбаматным пересыщениями, была исследована возможность применения указанного выше соотношения и к метастабильным растворам. Исследования показали, что это отношение удовлетворяет экспериментальным данным, если в уравнения подставить относительные концентрации НС03 и карбамата. [7]
Так как метастабильный раствор характеризуется кристаллизационным и карбаматным пересыщениями, была исследована возможность применения указанного выше соотношения и к метастабиль-ным растворам. Исследования показали, что это отношение удовлетворяет экспериментальным данным, если в уравнения подставить относительные концентрации HCOg и карбамата. [8]
Получен реакцией метастабильного раствора алюмината кальция с растворами кальциевых силикатов. [9]
Карбамид способен образовывать метастабильные растворы и в присутствии затравочных кристаллов. [10]
Выделение новой фазы из метастабильных растворов кристаллизующихся полимеров протекает во многом аналогично кристаллизации низкомолекулярных веществ. Скорость образования зародышей определяет скорость всего процесса кристаллизации. Рост пересыщения раствора или переохлаждения расплава повышает вероятность образования зародышей новой фазы лишь до определенного предела. По мере приближения к температуре стеклования подвижность молекул снижается, любые перегруппировки их тормозятся и скорость кристаллизации сильно уменьшается. [11]
 |
Схематическая диаграмма состояния бинарной системы полимер-растворитель. NI - молярная доля полимера ( в основных молях, N2 - молярная доля растворителя, Т - температура. [12] |
Область 3 также является областью метастабильных растворов ( За - жидких; ЗЪ - высокоэластичных; Зс - стеклообразных), но если в области 2 система разделяется на аморфные фазы - - разбавленный и концентрированный растворы полимера, то в области 3 она должна разделяться на кристаллический растворитель и стеклообразный полимер. [13]
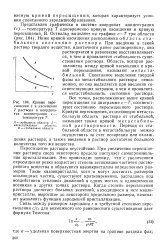 |
Кривые пересыщения 1 и насыщения 2 раствора в координатах концентрация с - температура Т. [14] |
Спонтанное выделение твердой фазы из метастабильного раствора невозможно, но она выделяется при введении соответствующих затравок, в чем и проявляется метастабильность состояния раствора. Все точки, расположенные выше кривой пересыщения на диаграмме с - Т, соответствуют состоянию пересыщенного раствора. Кривую пересыщения, отделяющую метаста-бильную область раствора от стабильной, называют также кривой метастабиль-ной растворимости. [15]
Страницы: 1 2 3 4