Рабочий раствор - нитрат
Cтраница 2
Полученный раствор вливают в смесь, содержащую 100 мл буферного раствора ( 750 г лимонной кислоты и 1 л концентрированного раствора гидроокиси аммония н а 1 л воды), 80 мл раствора гидроокиси аммония и избыток 0 05 N раствора КзРе ( СМ) б, и потенциометрически титруют избыток последнего 0 05 N рабочим раствором нитрата кобальта. [16]
Рабочий раствор готовят из запасного разбавлением в 10 раз, тщательно перемешивают и получают раствор, содержащий 0 01 мг N в 1 мл. Рабочий раствор нитрата калия не устойчив при хранении; поэтому его следует приготовлять непосредственно перед определением. [17]
Если титр рабочего раствора нитрата ртути был установлен по роданиду, то при точных определениях хлора необходимо ввести поправку на избыток рабочего раствора, пошедший на образование комплекса. [18]
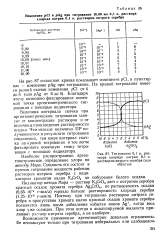 |
Титрование 0 1 н. рас. [19] |
Наиболее распространено арген-тометрическое определение хлора по методу Мора. Сущность его состоит в прямом титровании жидкости рабочим раствором нитрата серебра с индикатором хроматом калия К2СЮ4 до побурения белого осадка. [20]
Так как это не всегда выполнимо, часто прибегают к рода неметрическому методу определения хлора, пользуясь приемом обратного титрования. В этом случае ионы СГ сначала осаждают определенным объемом рабочего раствора нитрата серебра, а избыток последнего оттитровывают раствором роданида. Затем определяют, какое количество AgNO3 пошло на взаимодействие с СГ-ионами. [21]
Так как это не всегда выполнимо, часто прибегают к роданометрическому методу определения хлора, пользуясь приемом обратного титрования. В этом случае ионы СГ сначала осаждают определенным объемом рабочего раствора нитрата серебра, а избыток последнего оттитровывают раствором роданида. Затем определяют, какое количество AgNO3 пошло на взаимодействие с СГ-ионами. [22]
Раствор в мерной колбе тщательно перемешивают и отбирают пипеткой 25 мл в титровальную колбу или в стакан емкостью не менее 250 мл. К отобранному объему анализируемого раствора второй пипеткой прибавляют 50 мл рабочего раствора нитрата серебра. [23]
Пробу раствора хлорида натрия количественно переносят в мерную колбу на 100 мл, доводят дистиллированной водой до метки и перемешивают. Титрование проводят так же, как и при определении нормальности рабочего раствора нитрата серебра. [24]
Раствор в мерной колбе тщательно перемешивают и отбирают пипеткой 25 мл в титровальную колбу или в стакан емкостью не менее 250 мл. К отобранному объему анализируемого раствора второй пипеткой прибавляют 50 мл рабочего раствора нитрата серебра. [25]
Раствор в мерной колбе тщатель но перемешивают и отбирают пипеткой 25 мл в титровальную колбу или в стакан емкостью не менее 250 мл. К отобранному объему анализируемого раствора второй пипеткой прибавляют 50 мл рабочего раствора нитрата серебра. [26]
Раствор в мерной колбе тщательно перемешивают и отбирают пипеткой 25 мл в титровальную колбу или в стакан емкостью не менее 250 мл. К отобранному объему анализируемого раствора второй пипеткой прибавляют 50 мл рабочего раствора нитрата серебра. [27]
Раствор, содержащий иодид натрия и хлорид натрия, титруют рабочим раствором нитрата серебра с серебряным электродом. При этом обнаруживаются два скачка потенциала. Первый скачок потенциала соответствует окончанию осаждения иодида, второй - окончанию осаждения хлорида серебра. [28]
Раствор в мерной колбе тщательно перемешивают и отбирают пипеткой 25 мл в титровальную колбу или в стакан емкостью ае менее 250 мл. К отобранному объему анализируемого раствора при помоши второй пипетки прибавляют 50 мл рабочего раствора нитрата серебра. [29]
Нужно показать учащимся приемы титрования с выносным каломельным электродом, соединенным с анализируемым раствором через электролитический ключ - стеклянную U-образную трубку, заполненную раствором нитрата аммония. В стакан для титрования помещают анализируемый раствор хлорида натрия, добавляют раствор нитрата бария и затем титруют при размешивании рабочим раствором нитрата серебра до скачка потенциала. [30]
Страницы: 1 2 3