Слишком кислый раствор
Cтраница 1
Слишком кислые растворы нейтрализуют перед добавлением буферного раствора. После добавления каждой порции раствора комплексона измеряют величину светопоглощения и полученные значения наносят на график. [1]
Слишком кислые растворы могут временно ослабить волосы. Даже после сушки некоторый избыток ионов водорода остается в соседних цепях, мешая образованию новых водородных и ионных связей. [2]
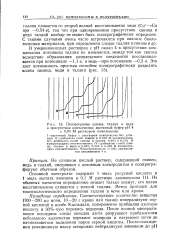 |
Подпрограмма свинца, таллия и меди. [3] |
Не слишком кислый раствор, содержащий свинец, медь и таллий, смешивают с основным электролитом и полярогра-фируют обычным образом. [4]
Не слишком кислый раствор, содержащий свинец, медь и таллий, смешивают с основным электролитом и полярографируют обычным образом. [5]
 |
Слоистая структура глин, пирофиллита и слюды. [6] |
В не слишком кислом растворе возможен обмен катионов на протоны. Кроме того, монтмориллонитовые глины способны к набуханию, что связано с влиянием ионной силы раствора на отталкивание двойных слоев ( см. разд. [7]
Если фотобумагу погружают в слишком кислый раствор или если она слишком долго лежала в обычном разбавленном растворе уксусной кислоты, то после ее сушки со стороны подложки, а иногда и на эмульсионной стороне появляются блестящие пятна. [8]
Щавелевая кислота осаждает из не слишком кислых растворов весь торий в виде белого кристаллического щавелевокислого тория, практически не растворимо го избытке щавелевой кислоты и разбавленных минеральных кислотах. [9]
Щавелевая кислота осаждает из не слишком кислых растворов весь торий в виде белого кристаллического щавелевокислого тормя, практически не растворимого избытке щавелевой кислоты и разбавленных минеральных кислотах. [10]
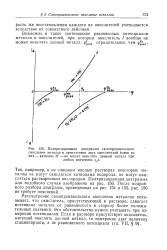 |
Поляризационная диаграмма самопроизвольного. [11] |
Так, например, в не слишком кислых растворах некоторые металлы не могут окисляться катионами водорода, но могут окисляться растворенным кислородом. После подробного разбора диаграмм, приведенных на рис. 154 и 155, рис. 156 не требует пояснений. [12]
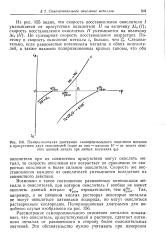 |
Поляризационная диаграмма самопроизвольного окисления металла в присутствии двух окислителей ( один из них - катионы Н - не может окислять данный металл при любых значениях рс. [13] |
Так, например, в не слишком кислых растворах некоторые металлы не могут окисляться катионами водорода, но могут окисляться растворенным кислородом. [14]
Тиосульфат натрия постепенно осаждает олово из не слишком кислых растворов. [15]
Страницы: 1 2