Совершенный ионный раствор
Cтраница 2
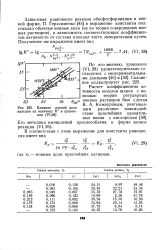 |
Влияние ионной доли кальция на величину К в уравнении. [16] |
Герасименко [45] в выражение константы подставлял обычные ионные доли ( не по теории совершенных ионных растворов), а зависимость соответствующих коэффициентов активности от состава находил чисто эмпирическим путем. [17]
В общем случае силикатный расплав не может быть отнесен ни к идеальному, ни к совершенному ионному раствору. [18]
В частности, поведение шлаков с малым содержанием катионов второй группы удовлетворительно согласуется с так называемой теорией совершенных ионных растворов, по которой активность компонента равна произведению ионных долей. Напротив, повышение концентрации катионов второй группы приводит к нарастающим отклонениям от этой теории. Добавки веществ, содержащих катионы первой группы, например СаО, заметно повышают активность ионов кислорода в шлаке, а введение соединений, включающих катионы второй группы, в частности SiO2, резко ее снижает. [19]
Например, активность MgO в шлаках, насыщенных ею, оказываемся более постоянной, чем вычисленная по теории совершенных ионных растворов. [20]
 |
Линии изоактивности в системе СаО - SiOj - AlOll5 при 1600 С. [21] |
Необходимо подчеркнуть, что в отсутствие иных атомных анионов, чем кислород, отклонения расплавленного шлака от идеальных и от совершенных ионных растворов могут быть достаточно большими. [22]
Согласно понятию о микронеоднородности, энергетическая неравноценность ионов должна вызвать дополнительное упорядочение в расположении частиц по сравнению с так называемыми совершенными ионными растворами, в которых распределение ионов статистически равномерно. В противоположность последним распределение ионов в реальных жидких шлаках, а также в расплавленных солях оказывается неравномерным. Обычно энергия взаимодействия одних ионных пар заметно превосходит все остальные. Такие частицы будут чаще находиться в соседстве одна с другой и могут образовывать свои группы. [23]
Поэтому, говоря о шлаках, важно отметить, что энергетическая неравноценность ионов вызывает дополнительное упорядочение в расположении частиц по сравнению с совершенными ионными растворами. В противоположность последним, распределение ионов в жидком шлаке может оказаться неравномерным. [24]
Наряду с ионными долями в выражения для / Cs, LS и LQ приходится ввести коэффициенты активности ys2 и - iQz -, показывающие степень отклонения реального шлака от совершенного ионного раствора. [25]
Например, А. М. Самарин и Л. А. Шварцман [272] нашли, что произведение растворимости СаО и MgO для расплавов различных составов имеют одинаковый порядок величины при заданной температуре, если вычислять активности ионов по теории совершенных ионных растворов. [26]
Выражение ( VI, 20) не совсем точно, так как в формуле ( VI, 19) ионные доли подсчитаны обычным путем, а в уравнении (VI.7) - по теории совершенных ионных растворов. [27]
Совершенный ионный раствор характеризуется следующими признаками: 1) он состоит только из ионов; 2) близлежащими соседями в нем, как и в кристалле, являются только ионы разного знака; 3) энергия взаимодействия между ионами в растворе остается такой же, как и в отдельно взятых чистых компонентах. От идеального совершенный ионный раствор отличается вторым признаком, предусматривающим существование определенного порядка в расположении частиц. [28]
При более высоких концентрациях SiO2 оно приводит к результатам, качественно противоположным наблюдающимся на опыте. Таким образом, теория совершенных ионных растворов не описывает распределение кислорода между металлом и шлаком. Между тем предположение о существовании химических соединений в шлаках, по крайней мере качественно, позволяет решить эту задачу более удовлетворительно. В химической теории учитывается разница в кислотно-основных свойствах оксидов. Так, например, энтальпия реакции 2CaOT SiO2T Ca2SiO4T составляет - 143 кДж / моль, а реакции 2FeOT - T - SiO2T Fe2SiO4T всего лишь около 46 кДж / моль. Это позволяет предполагать, что в расплаве ионы Са2 преимущественно располагаются вблизи крем-нийкислородных анионов, образуя как бы молекулы силиката кальция. Допуская, что в шлаке образуются молекулы Ca2SiO4, можно получить приблизительно правильное описание распределения кислорода между железом и шлаком. [29]
Расплавы солей, окислов и сульфидов представляют собой, по терминологии, предложенной Темкиным [1], ионные растворы. Темкиным было введено также понятие совершенных ионных растворов и рассмотрена термодинамика их. [30]
Страницы: 1 2 3