Титруемый раствор
Cтраница 3
Титруемый раствор щавелевой кислоты или оксалата натрия должен быть горячим. Если к концу титрования раствор остынет, его вновь нагревают, но не доводят до кипения. Если вместо розовой окраски получится коричневато-бурая, это значит, что при титровании допущена какая-то ошибка, и опыт следует повторить. [31]
Титруемый раствор щавелевой кислоты или оксалата натрия должен быть горячим. Если к концу титрования раствор остынет, его вновь нагревают, но не доводят до кипения. Если вместо розоватой окраски получится коричневато-бурая, то это следует считать следствием какого-либо упущения во время титрования. [32]
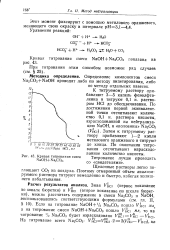 |
Кривая титрования смеси NaOH4 - Na2CO3. [33] |
Затем титруемому раствору прибавляют 1 - 2 ка пли метилового оранжевого и титруют до конца. По окончании титрования отсчитывают израсходованное количество кислоты. [34]
В титруемый раствор погружают на 50 мм алюминиевый и нихромовый электроды, предварительно тщательно отполированные и протертые увлажненной фильтровальной бумагой. [35]
Если титруемый раствор очень темен, то вместо фенолфталеина лучше применять тимолсиний или этил-бис - ( 2 4-динитрофенил) - ацетат. В этих случаях было предложено вводить в раствор хлорид бария 2; при этом осаждается бариевое мыло, уносящее с собой окрашенные вещества. Затем смесь разбавляют до определенного объема водой и титруют аликвотную часть прозрачной жидкости. При этом, однако, неизбежна ошибка, так как бариевое мыло захватывает и некоторое количество едкой щелочи. [36]
Если титруемый раствор не дотитрован, то проба с AgNOa мутнеет, а проба, в которой находится определяемое вещество, е мутнеет. Если титруемый раствор перетитршан, то мутнеет ( Проба при добавлении к ней определяемого иона. В момент, когда Величина [ Ag ] станет равной величине [ Ап -, обе пробы мутнеют в одинаковой мере. [37]
Если титруемый раствор дает окрашенный вытек, к раствору прибавляют 5 - 7 г поваренной соли. [38]
В титруемый раствор опускают два инертных ( платиновых) электрода. После введения каждой порции титранта измеряют электропроводность раствора и по полученным данным строят график зависимости электропроводности от объема добавленного титранта. [39]
Если титруемый раствор дает окрашенный вытек, к раствору прибавляют 5 - 7 г поваренной соли. [40]
В титруемый раствор погружают два одинаковых электрода в виде небольших платиновых пластинок или проволок. К ним прикладывают низкое напряжение ( 10 - 15 мв) от сухого элемента. [41]
Когда титруемый раствор из бурого превращается в соломенно-желтый, добавляют 2 - 3 мл 0 2 % - ного раствора крахмала. От прибавления крахмала раствор приобретает сине-черный цвет. Раствор продолжают титровать до исчезновения синей окраски. Расчет производят по уравнению ( 36) ( см. стр. [42]
 |
Типы водородных электродов. [43] |
В титруемый раствор погружают плати - новый электрод в виде пластинки или сетки и прибавляют немного хингидрона. Титрование ведется при перемешивании. [44]
В титруемый раствор можно опустить платиновый электрод и соединить раствор с нормальным водородным электродом полупроницаемой перегородкой подобно тому, как описано выше, при рассмотрении вопроса об окислительном потенциале. [45]
Страницы: 1 2 3 4