Переохлажденный раствор
Cтраница 1
Переохлажденный раствор попадает в ресивер, в паровом пространстве которого поддерживается давление рп благодаря тому, что пары находятся в равновесном состоянии с пленкой насыщенного раствора, находящегося на поверхности крепкого раствора в ресивере. [1]
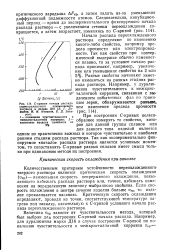 |
С-кривые начала распада ЦЗМ ЗСрвН, ОбнаруЖИВЗвТСЯ рЗНЬШв. [2] |
Начало распада переохлажденного раствора определяют по изменению какого-либо свойства, например предела прочности или электропроводности. Разные свойства начинают заметно изменяться на разных стадиях распада раствора. [3]
Поступающий к зеркалу АА переохлажденный раствор поглощает пары из парового пространства. При этом на поверхности зеркала образуется тонкая пленка насыщенного раствора, который находится в равновесии с паром. [4]
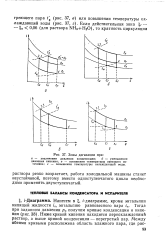 |
Зоны дегазации при. [5] |
Ниже кривой кипения находится переохлажденный раствор, а выше кривой конденсации - перегретый пар. [6]
Для пересыщен ного или переохлажденного раствора приведенные уравнения несколько видоизменяются. [7]
Кристаллизация азотнокислого кальция из переохлажденного раствора наступает лишь при внесении затравки и в дальнейшем протекает достаточно быстро. [8]
Для хранения и транспортировки переохлажденных растворов ацетилена в ацетоне, возможно, найдут применение также емкости, в которых в качестве промежуточного хладагента рекомендован жидкий метан. [9]
Кристаллизация из слабо пересыщенных или переохлажденных растворов сопряжена с образованием сравнительно небольшого числа центров роста. Поэтому азотные удобрения, по идее, должны состоять из кристаллов сравнительно крупного размера. [10]
Если, однако, тепловая подвижность атомов переохлажденного раствора недостаточна, то состояние пересыщения может сохраняться неопределенно долгое время. [11]
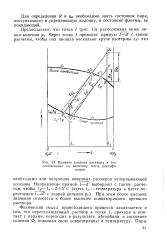 |
Влияние кипения раствора в теплообменнике на величину тепла ректификации. [12] |
Физический смысл происходящего процесса заключается в том, что переохлажденный раствор в точке /, приходя в контакт с парами, переходит в результате абсорбции в состояние кипения Ф, повышая свою концентрацию и температуру. [13]
Тиосульфат натрия важен для демонстрации выделения теплоты при кристаллизации переохлажденного раствора. Эта соль необходима также при работах по фотографии для фиксирования и, в частности, с ее помощью можно сделать прозрачной фотографическую непроявленную пластинку, что нужно, например, при изготовлении рисованных диапозитивов. [14]
Зародыши, или центры, кристаллизации образуются из пересыщенных или переохлажденных растворов самопроизвольно. [15]
Страницы: 1 2 3 4