Добавленный раствор
Cтраница 3
А - поправочный коэффициент, на который нужно умножить измеренную активность раствора; V - начальный объем раствора; V0 - объем добавленного раствора осадителя. [31]
Вычерчивают кривую титрования, откладывая на оси ординат показания потенциометра в милливольтах или в единицах рН, а на оси абсцисс - объем добавленного раствора в кубических сантиметрах. За точки эквивалентности принимают точки перегиба кривой титрования, которые, как правило, находятся вблизи потенциалов, соответствующих буферных растворов. [32]
При добавлении серной кислоты или раствора хлорида, например кальция или магния, к разбавленному раствору соляной кислоты состав азеотропа изменяется в зависимости от количества добавленного раствора. [33]
К слабокислому раствору бихромата объемом около 25 мл добавляют раствор соли Мора до перехода окраски в зеленую и дополнительно 5 мл избытка, точно замечая объем добавленного раствора. Приливают раствор Нз5О4 ( 1: 1) для создания концентрации H2SO4, равной примерно 2 М, вводят 4 - 5 капель индикатора ( дифениламина) и 5 мл концентрированной фосфорной кислоты. Титруют стандартным раствором 1 / 60 М К2Ст2О7 до перехода окраски индикатора в пурпурную. Затем продолжают титрование раствором соли Мора и стандартным раствором бихромата, как описано выше. Объем раствора Ре, пошедшего на титрование, соответствует содержанию бихромата в смеси. [34]
При кондуктометрическом титровании раствор помещают в измерительную ячейку с подходящими электродами ( электроды из платинированной платиновой жести) и изучают изменение сопротивления или электропроводности как функцию количества добавленного раствора. [35]
Установленные во второй части работы значения рН растворов, содержащих салицилат натрия, наносят на график в координатах рН - DHCI, где L HCI ( мл) - общий объем добавленного раствора, содержащего соляную кислоту. [36]
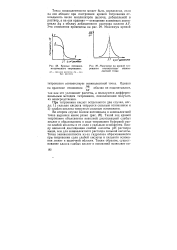 |
Кривые потенциометр ического титрования.| Максимум на кривой титрования соответствует эквивалентной точке. [37] |
Точка эквивалентности может быть определена, если на оси абсцисс при построении кривой титрования откладывать число миллилитров щелочи, добавляемой в раствор, а на оси ординат - отношение изменения потенциала Аф к объему добавленного раствора щелочи AF. [38]
В колбу наливают из бюретки 1 мл исследуемого латекса и разбавляют его раствором стабилизатора ( 0 1 % - ным аммиачным раствором лейканола) до тех пор, пока мутность латекса не будет казаться на глаз такой же, как и мутность стандартного латекса известной концентрации. Записывают объем добавленного раствора стабилизатора и рассчитывают кратность разбавления. [39]
Если анализируемая вода имеет кислую или щелочную реакцию, к пробе добавляют раствор щелочи или кислоты до слабокислой реакции по индикаторной универсальной бумаге. Обычно объем добавленного раствора щелочи или кислоты бывает незначителен, поэтому происходящее при этом разбавление пробы не учитывают. [40]
Добавляют из бюретки раствор сульфата серебра ( 4 4 г / дм3) объемом ( 0 05 са) см3, где са - ранее определенное содержание хлорида. Записывают объем добавленного раствора сульфата серебра. [41]
Отмечают объем добавленного раствора РеСЬ - Далее добавляют к той же пробе еще раствор FeCls до тех пор, пока окраска не станет такой же как раствора с неочищенным К. Снова отмечают объем добавленного раствора FeCls. По объемам добавленного раствора FeCl3 рассчитывают содержание FeCls в неочищенном и очищенном образцах хлорида калия. [42]
Точки титрования соответствуют объемам добавленного раствора NaOH - 0; 10; 50; 75; 100 мл. [43]
 |
Изменение рН в процессе титрования 50 00 мл 0 1000 F раствора хлористоводородной кислоты 0 1000 F раствором гидроксида натрия. [44] |
После достижения точки эквивалентности мы добавляем избыток титранта - гидроксида натрия к раствору хлорида натрия. Имеется два источника гидроксид-ионов - добавленный раствор гидроксида натрия и автопротолиз воды. [45]
Страницы: 1 2 3 4