Неводный раствор
Cтраница 3
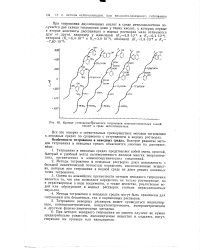 |
КРивые потенциометрического титрования многокомпонентных смесей кислот в среде метилэтилкетона. [31] |
Титрование неводных растворов может проводиться индикаторным, потенциометрическим, кондуктометрическим, амперометрическим и другими физико-химическими методами. [32]
Использование неводных растворов позволяет получать путем электролиза металлы, выделение которых невозможно в водных растворах, так как при достаточно отрицательных потенциалах электрода основной реакцией является выделение водорода. [33]
Титрование неводных растворов можно осуществлять индикаторным, потенциометрическим, кондуктометрическим, ампе-рометрическим и другими физико-химически: и методами. [34]
Применение неводных растворов имеет значение для очистки органических жидкостей от примесей и для органического катализа. [35]
Электропроводность неводных растворов обычно значительно меньше электропроводности водных. Исключение составляют аммиачные растворы, а также растворы в HCN, где электропроводность гораздо выше, чем в водных. В табл. XVII, 4 приведены значения электропроводности растворов НС1 в разных растворителях, а также диэлектрические проницаемости этих растворителей. [36]
 |
Кривые потенциометрического титрования многокомпонентных смесей кислот в среде метилэтилкетона. [37] |
Титрование неводных растворов может проводиться индикаторным, потенциометрическим, кондуктометрическим, амперометрическим и другими физико-химическими методами. [38]
Использование неводных растворов позволяет получать путем электролиза металлы, выделение которых невозможно в водных растворах, так как при достаточно отрицательных потенциалах электрода основной реакцией является выделение водорода. [39]
Для неводных растворов в качестве стандартного состояния растворителя берется чистое жидкое состояние этого компонента при данной температуре. [40]
Деминерализация неводных растворов ( таких, как спирт, жидкий аммиак), судя по измеренным в этих растворах свойствам мембран, представляется возможной, хотя длительная стабильность ионоселективных мембран в этих средах еще не подтверждена. [41]
Для неводных растворов в качестве стандартного состояния растворителя берется чистое жидкое состояние этого компонента при данной температуре. [42]
Исследованию неводных растворов и созданию единой теории диссоциации сильных и слабых электролитов в водных и неводных растворах посвящены современные работы кафедры физической химии Харьковского университета. [43]
Из неводных растворов с помощью электролиза выделяется магний - металл, получение которого в промышленности сопряжено с необходимостью вести электролиз высокотемпературных расплавов. При электролизе неводных растворов солей магния одновременно с солями других металлов можно получать магниевые сплавы, применение которых в технике столь полезно и столь разнообразно. [44]
Для неводных растворов неприменимы обычные представления о кислотах и щелочах в водных растворах, согласно которым кислотой называется химическое соединение, диссоциирующее в растворе на анион и ион водорода ( гидроксония), и основанием - соединение, диссоциирующее на катион металла и ион гидроксила. [45]
Страницы: 1 2 3 4