Концентрированный раствор - сульфит - натрий
Cтраница 1
 |
Плотность растворов NaHSO3 при 15 С. [1] |
Концентрированные растворы сульфита натрия не разлагаются даже при 16-часовом нагревании до 150 С. [2]
Процесс получения концентрированного раствора сульфита натрия ничем не отличается от описанного ранее процесса получения семиводного сульфита натрия ( стр. Полученный раствор затем очищают от примесей путем подщелачивания каустической содой. При достижении определенной щелочности раствора примесь железа выпадает сначала в виде гидрата закиси железа, которая, окисляясь, переходит в осадок гидрата окиси железа. [3]
Производство семиводного сульфита натрия заключается в получении концентрированного раствора сульфита натрия и кристаллизации из этого раствора семиводного сульфита натрия. [4]
Производство безводного сульфита натрия сводится к получению концентрированного раствора сульфита натрия и кристаллизации из него безводного сульфита натрия. [5]
Производство безводного сульфита - натрия сводится к получению концентрированного раствора сульфита натрия и кристаллизации из него при нагревании безводной соли. [6]
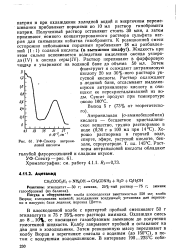 |
УФ-Спектр антрани - спирте, эфире, уксусной кислоте, бен-ловой кислоты золе, сероуглероде. Т. пл. 145 С. Раст. [7] |
Полученный раствор оставляют стоять 30 мин, а затем приливают немного концентрированного раствора сульфита натрия для связывания избытка гипобромита. К реакционной смеси осторожно небольшими порциями прибавляют 18 мл разбавленной ( 1: 1) соляной кислоты ( в вытяжном шкафу. Раствор переливают в фарфоровую чашку и упаривают на водяной бане до объема 50 мл. [8]
При пропускании удушливого газа А через бромную воду выпадает осадок простого вещества В, которое растворяется в концентрированном растворе сульфита натрия с образованием соли С. При приливании раствора соли С к осажденным галогенидам серебра образуется прозрачный раствор. [9]
Для определения иода к раствору после разложения, содержащему иод в виде иодата серебра, прибавляют 200 мл воды и немного нитрата аммония для предотвращения образования трудно растворимых даже в кислотах кристаллов хромата серебра, загрязняющих иодид серебра. Затем прибавляют концентрированный раствор сульфита натрия и восстанавливают иодат и хромовую кислоту. Выпадает осадок иодида серебра, а раствор становится светло-зеленым. Иодид серебра отфильтровывают через фильтрующий тигель, промывают и взвешивают. Если осадок иодида серебра окрашен в серый цвет металлическим серебром, образовавшимся вследствие того, что прибавлено слишком много сульфита или содержимое колбы при восстановлении было теплым, то осадок кипятят с 10 % - ным раствором азотной кислоты, смывают иодид серебра горячей водой в тигель и хорошо промывают. [10]
После спуска осветленного концентрированного раствора сульфита натрия в кристаллизатор включают механическую мешалку и подают пар в змеевик для нагрева раствора. При повышении температуры растворимость сульфита натрия уменьшается и некоторая часть его выпадает из раствора в виде безводных кристаллов. Большая же часть сульфита натрия остается растворенной в маточном растворе. Процесс нагрева раствора и выделения кристаллов продолжается около 1 часа. Получается пульпа, представляющая собой взвесь кристаллов в маточном растворе. Пульпу спускают в нутч-сушилку для отделения кристаллов от маточного раствора и сушки их. [11]
После спуска осветленного концентрированного раствора сульфита натрия в кристаллизатор включают механическую мешалку и подают пар в змеевик для нагрева раствора. Нагревают раствор до 95 - 100 С. Большая же часть сульфита натрия остается растворенной в маточном растворе. Процесс атрева раствора и выделения кристаллов продолжается околи 1 час. Получается суспензия, представляющая собой взвесь кристаллов в маточном растворе. [12]
Исключением является только метол, который в концентрированных растворах сульфита натрия растворяется очень плохо. [13]
Моделирование потребления кислорода может производиться и при поддержании определенной концентрации растворенного в воде кислорода. В этом случае в аэрируемый объем жидкости непрерывно дозируется концентрированный раствор сульфита натрия с катализатором. Количество подаваемого восстановителя подбирается таким образом, чтобы концентрация растворенного кислорода в период установившегося равновесия составляла. Величина окислительной способности может быть вычислена по скорости окисления сульфита натрия с корректировкой на дефицит кислорода. Эта методика позволяет получить более точные результаты, так как реакция окисления происходит главным образом в объеме жидкости, а не на поверхности раздела фаз, однако количество измерений по этому способу значительно больше и эксперименты требуют много времени. [14]
К концу операции продувают через раствор воздух. После этого разбавляют до 300 - 400 мл, фильтруют и восстанавливают в фильтрате иодат, прибавив концентрированный раствор сульфита натрия в таком количестве, чтобы спустя 10 мин. Большой избыток SO2 может вызвать восстановление иодида серебра. [15]
Страницы: 1 2