Разбавленный раствор - соль
Cтраница 1
Разбавленные растворы солей образуют большие потоки сточных вод. На 1 т катализатора, включая производство цеолита, расходуется свыше 2 т реагентов. Очистка ( деминерализация) сточных вод с утилизацией солей требует строительства сложных энергоемких установок, что значительно удорожает катализатор. [1]
Разбавленные растворы солей, кислот и оснований требуемой концентрации специально готовят. Их плотность обычно близка к единице. Концентрация этого раствора составляет 4: 1000 0 04 г / мл. Если для осаждения катионов кальция требуется 2 г ( NH4) 2C2O4, то нужно взять 200: 0 04 50 мл приготовленного раствора. [2]
Разбавленные растворы солей церия ( IV) более устойчивы, чем разбавленные растворы перманганата, и ими можно титровать и в солянокислой среде. [3]
Разбавленный раствор соли церия ( III) при обработке карбонатом калия образует белый осадок карбоната церия, растворимый в избытке осадителя. При стоянии раствор становится желтым, так как при окислении воздухом образуется комплексное соединение карбоната и перекиси церия. Желтая окраска появляется сразу, если добавляют перекись водорода. Ура при тех же условиях дает желтую или желто-оранжевую окраску. [4]
Разбавленные растворы солей церия ( IV) более устойчивы, чем разбавленные растворы перманганата, и ими можно титровать и в солянокислой среде. [5]
Разбавленные растворы солей аммония более агрессивны, чем такие же растворы хлоридов щелочных металлов. [6]
Если разбавленные растворы солей золота медленно восстанавливать органическими реагентами, то они приобретают красивый красный цвет и в полученном растворе можно обнаружить металлическое золото в мелко диспергированной форме, при этом частицы золота оказываются электрически заряженными и имеют примерно сферическую форму. Эти частицы не задерживаются бумагой при обычном фильтровании, однако они не проходят через пергаментную мембрану, поэтому раствор можно очистить методом диализа. [7]
Если разбавленные растворы солей слабых оснований и сильных кислот пропускать через анионит, то благодаря удалению кислоты равновесие гидролиза соли будет смещаться. [8]
Из разбавленных растворов солей мышьяковой и фосфорной кислот выпадают отдельные кристаллы ( см. рис. 14, стр. O отличается от соответствующей соли фосфорной кислоты отношением к нитрату серебра. [9]
 |
Кристаллы Cu [ Hg ( SCN4 ]. [10] |
Из разбавленных растворов солей меди в присутствии ионов Zn2 выделяются кристаллы, окрашенные в фиолетовый цвет. [11]
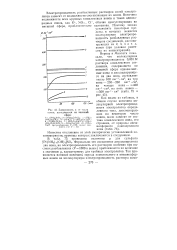 |
Зависимость fx от числа. [12] |
Электропроводность разбавленных растворов солей электролитов зависит от подвижности составляющих их ионов. Величина подвижности всех крупных комплексных ионов и таких однозарядных ионов, как К, МОз, С1 -, обычно присутствующих во внешней сфере, приблизительно одинакова. [13]
Из разбавленных растворов солей лития, содержащих меньше 0 01 г. мл, осадок не выпадает. [14]
Электропроводность разбавленных растворов солей слабых кислот не пропорциональна Их концентрациям в отличие от нейтральных солей, где эта пропорциональность сохраняется. Это приводит к неточности при определении солесодержания котловой воды при измерении ее электропроводности, так как эта вода содержит обычно карбонат натрия, а иногда фосфат натрия; возникающая при этом ошибка, однако, несущественна. [15]
Страницы: 1 2 3 4