Очень разбавленный раствор - кислота
Cтраница 2
Для очень разбавленных растворов кислот и щелочей, концентрация которых приближается к концентрации [ Н ] и [ ОН - ] в чистой воде, уже нельзя пренебрегать диссоциацией воды. [16]
Часто возникает необходимость титровать очень разбавленные растворы кислот щелочью и обратно титровать кислотой очень разбавленные растворы щелочей. Чтобы исключить в таких случаях влияние углекислого газа, можно производить титрование при температуре кипения, применяя в качестве индикатора фенолкрасный, крезолкрасный, бромти-молсиний или даже метал - красный. В таких определениях следует, конечно, пользоваться посудой из химически стойкого стекла, чтобы избежать извлечения из нее щелочей. [17]
С другой стороны, в очень разбавленных растворах кислот скорость разложения снова возрастает вместе с увеличением концентрации водородных ионов. [18]
Следует тут же отметить, что расчеты рН для очень разбавленных растворов кислот и оснований практического смысла не имеют, так как концентрации таких растворов очень быстро меняются за счет контакта со стенками посуды и воздухом, в котором всегда содержится угольный ангидрид. [19]
 |
Изменение электро - непосредственно по электропроводности ра-проводности при титровании. створа можно HenpepbIBHO следить за содержанием СО2 в печном газе. [20] |
Кондуктометрический метод имеет некоторые преимущества перед другими методами при титровании очень разбавленных растворов кислот и оснований, а также при некоторых реакциях осаждения. Этот метод применяется также при титровании окрашенных или мутных растворов. [21]
Даже в этом крайнем случае, когда мы имеем дело с очень разбавленным раствором кислоты с двумя близкими ступенями ионизации, второе приближение вполне удовлетворительно. [22]
Обычно мы прибавляем при исследовании рН раствора очень малое количество индикатора, что вполне достаточно благодаря его интенсивной окраске. Однако необходимо помнить, что в очень разбавленных растворах кислот и оснований существенную роль играют кислотные или основные свойства самого индикатора. Если мы к нескольким каплям индикатора добавим одну каплю разбавленного раствора кислоты или основания, то рН смеси этого раствора и индикатора будет в значительной степени зависеть от константы диссоциации индикатора. В таком случае смещение равновесия диссоциации индикатора оказывается недостаточным, а результат измерения ошибочным. [23]
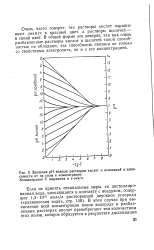 |
Значения рН водных растворов кислот и оснований в зависимости от их силы и концентрации. Концентрация С выражена в г-экв / л. [24] |
Очень часто говорят, что растворы кислот окрашивают лакмус в красный цвет, а растворы щелочей - в синий цвет. В общей форме это неверно, так как очень разбавленные растворы кислот и щелочей такой способностью не обладают, эта способность связана не только со свойствами электролита, но и с его концентрацией. [25]
В табл. 3 - 1 приведены значения [ О 1 ] и рН, рассчитанные для различных концентраций сильной кислоты. Из сравнения данных граф - lg С д и рН ясно следует, в каком интервале концентраций кислот можно применять упрощенную формулу. Для концентраций ниже 10 - 7 М упрощенная формула ведет к ошибочному заключению, что очень разбавленные растворы кислот имеют основную реакцию. Из этих данных следует также, что для концентраций порядка 10-в М единственным значащим фактором является диссоциация воды. [26]
Страницы: 1 2