Предыдущий раствор
Cтраница 3
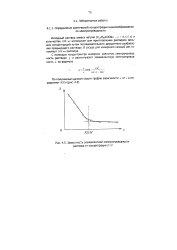 |
Зависимость эквивалентной электропроводности раствора от концентрации ПАВ. [31] |
Исходный раствор олеата натрия ( С НззСООМа, с 0 125 н в количестве 100 ш используют для приготовления растворов меньших концентраций путем последовательного двукратного разбавления предыдущего раствора. В сосуде для измерения каждый раз оставляют 100мл раствора. [32]
Эталонные растворы кальция в воде, содержащие 0 4; 0 8; 1 6; 3 2 и 6 4 мкг / мл кальция, готовят разбавлением предыдущего раствора. [33]
Одним из существенных недостатков потенциометрического метода измерения концентрации растворов является необходимость тщательной промывки измерительной ячейки ( датчика рН - метра) после анализа каждой пробы, так как даже ничтожные количества предыдущего раствора, оставшегося на поверхности датчика, приводят к ошибкам измерения концентрации последующего раствора. [34]
Одним из существенных недостатков потенщюметрического метода измерения концентрации растворов является необходимость тщательной промывки измерительной ячейки ( датчика рН - метра) после анализа каждой пробы, так как даже ничтожные количества предыдущего раствора, оставшегося на поверхности датчика, приводят к ошибкам измерения концентрации последующего раствора. [35]
 |
График для определения констант в уравнении Фрейндлиха. [36] |
Следует заметить, что до адсорбции от - Таблица 5 титровывают только исходный раствор, и содержание вещества в более разбавленных растворах вычисляют посредством уменьшения в два раза количества вещества, содержащегося в 50 см3 предыдущего раствора. [37]
В табл. 8 приведены номера основ буровых растворов и количество химических реагентов ( в т / м8), необходимое для перевода из основы в основу, независимо от того, какими химическими реагентами был обработан предыдущий раствор. [38]
Реактивы: n - нитрофенилфосфат натрия, 0 4 % - ный раствор в 0 001 моль / л растворе соляной кислоты; глициновый буфер, 0 05 моль / л раствор, содержащий катализатор - клорид магния ( 10 мг / дл); субстратно-буферный раствор ( рН 10 5) готовят смешиванием равных частей двух предыдущих растворов; NaOH, 0 02 моль / л раствор. [39]
Солянокислый раствор эфира ( плотн. Приготовляется аналогично предыдущему раствору. [40]
 |
Форма записи результатов определения порогов коагуляции при различных концентрациях электролита ( в моль / л. [41] |
Оставшихся 4 мл раствора концентрации а недостаточно для проведения необходимых разбавлений. Поэтому из предыдущего раствора электролита с концентрацией в десять раз выше пороговой ( 10 а) готовят 10 мл раствора, соответствующего верхнему пределу грубого порога, и добавляют их-к оставшимся 4мл такого же раствора. Из суммарного количества раствора электролита ( 14 мл) отбирают в четыре пробирки 4, 3, 2 и 1 мл и добавляют к ним соответственно 1, 2, 3 и 4мл дистиллированной воды. Затем в каждую пробирку приливают по 5 мл золя и наблюдают коагуляцию. [42]
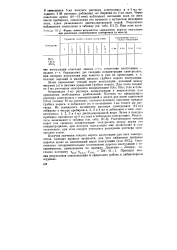 |
Форма записи результатов определения порогов коагуляции при различных концентрациях электролита ( в моль / л. [43] |
Оставшихся 4 мл раствора концентрации а недостаточно для проведения необходимых разбавлений. Поэтому из предыдущего раствора электролита с концентрацией в десять раз выше пороговой ( 10 а) готовят 10 мл раствора, соответствующего верхнему пределу грубого порога, и добавляют их к оставшимся 4 мл такого же раствора. Из суммарного количества раствора электролита ( 14 мл) отбирают в четыре пробирки 4, 3, 2 и 1 мл и добавляют к ним соответственно 1, 2, 3 и 4мл дистиллированной воды. Затем в каждую пробирку приливают по 5 мл золя и наблюдают коагуляцию. Рассчитывают точный порог как среднюю концентрацию электролита между двумя его концентрациями, при которых коагуляция еще происходит и уже отсутствует, при этом следует учитывать разведение раствора электролита золем. [44]
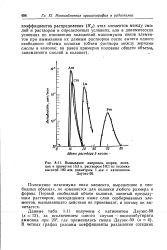 |
Вымывание америция, кюрия, лютеция и прометия 13 3 н. раствором НС1 из колонки высотой 100 мм, диаметром 1 мм с катионитом Дауэкс-50. [45] |
Страницы: 1 2 3 4