Определяемый раствор
Cтраница 3
При анализе следов приходится иметь дело или с малыми количествами веществ, или с очень низкими концентрациями определяемых растворов. В первом случае, если возможности классических методов исчерпаны, следует использовать линейную ТСХ с большей динамической областью. [31]
Перед началом титрования строят характеристическую кривую прибора ( рис. 35) и по ней выбирают область рабочих концентраций определяемых растворов и способы настройки прибора. [32]
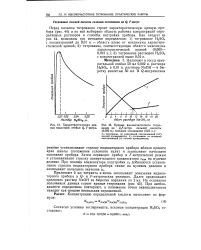 |
Характеристическая кривая емкостной ячейки Q, F-метра.| Кривые высокочастотного титрования на Q. F-метре сильной кислоты ( 0 002 н. сильным основанием ( 0 01 н.. [33] |
Перед началом титрования строят характеристическую кривую прибора ( рис. 44) и по ней выбирают область рабочих концентраций определяемых растворов и способы настройки прибора. [34]
Например, навеску КЮ3 растворяют в воде и обрабатывают избытком раствора KI и Na2S2O3 5НаО Полученный раствор титруют определяемым раствором кислоты в присутствии метилового красного. Пока в растворе имеется КЮ3, среда его будет нейтральная; первая избыточная капля кислоты сделает раствор кислым и окрасит метиловый красный в красный цвет. [35]
Например, навеску КЮ8 растворяют в воде и обрабатывают избытком раствора К1 и Na2S2O3 5НгО Полученный раствор титруют определяемым раствором кислоты в присутствии метилового красного. Пока в растворе имеется КЮ3, среда его будет нейтральная; первая избыточная капля кислоты сделает раствор кислым и окрасит метиловый красный в красный цвет. [36]
Следует познакомить учащихся и с другими приемами измерения оптической плотности, когда в правый световой поток сначала вводят кювету с определяемым раствором ( и в этом положении настраивают прибор на начало отсчетов), а затем заменяют ее кюветой с раствором сравнения и уравнивают световые потоки. Отсчет в этом случае ведут по левому барабану. [37]
Расчет выполняют обычным порядком, но следует обратить внимание на то, что титрование в этом случае ведут не рабочим, а определяемым раствором. [38]
В табл. 4.1 представлены относительные ошибки титрования для различных соотношений величин А, С, К и г в присутствии мешающего иона только в определяемом растворе. [39]
В качестве базовой конструкции служит электрод с жидкой мембраной фирмы Орион с пористой мембраной от электрода модели 92 - 19, отделяющей органическую фазу от определяемого раствора. Водный раствор сравнения представляет собой смесь 0 1 М растворов хлорида и салицилата натрия. Электроды подготавливают к работе, погружая их на ночь в водный 0 2 М раствор салицилата натрия. [40]
Как известно, можно количественно осадить натрий в виде уранил-цинк-натриевого ацетата в присутствии солей кальция, магния, бария, а также и калия, если присутствует меньше 50 мг хлористого калия на 1 мл определяемого раствора. [41]
Разность объемов HjSC, пошедших на титрование в первом и во вто - Ззом случаях, отнесенная в случае необходимости к 1 мл раствора фенилли-тия и умноженная на 0 1 и фактор пересчета HzSC, представляет собой нормальность определяемого раствора. [42]
Высокая чувствительность ( 0 01 - 0 02 мкг / мл) была достигнута в [70]; свет от источника излучения-бактерицидной ртутной лампы БУВ-15 или ртутной лампы высокого давления ПРК-2, работающей в режиме тлеющего разряда, пройдя через газовую кювету, в которую подается определяемый раствор и раствор восстановителя SnCl2, попадает на фотоумножитель ФЭУ-20, перед фотокатодом которого укреплена комбинация светофильтров и люминофора; в качестве люминофора берется Zn2SiO4 - Mn или смесь, используемая в лампах дневного света; светофильтры: ЖС-17 и СЗС-10. Над горелкой укрепляется трубка из железа или латуни диаметром 1 5 - 2 0 см и длиной 22 - 68 см. Давление воздуха 0 7 кг / см2, количество пропан-бутана берется таким, чтобы получить бледное, едва светящееся пламя; стабилизатор ВСМ-1; напряжение 1 2 - 1 4 кв; регистратор излучения - микроамперметр М-95; определение ведется по линии Hg 2537 А. [43]
Определяемый раствор иода помещают в мерную колбу на 100 мл и доводят водой до метки. Мора переносят в коническую колбу и разбавляют водой до объема 60 - 70 мл. Когда смесь в колбе станет светло-желтой, добавляют 2 мл раствора крахмала и продолжают медленно титровать до исчезновения синей окраски. Получив 2 - 3 сходящихся результата, рассчитывают количество иода в растворе. [44]
 |
Градуировочный график. [45] |
Страницы: 1 2 3 4