Водный раствор - реагент
Cтраница 1
Водный раствор реагента имеет розовый цвет. Не мешают большие количества ионов аммония, Li, К, Na, Ag, Ca, Sr, Ba, Mg, Zn, Cd, Hgn, SnIV, Pb, Vv, Mo, Co, Ni, а также хлорид-ионы. Мешают фосфат -, пирофосфат -, фторид - и вольфрамат-ионы; они маскируют ионы лантанидов. [1]
Водный раствор реагента поглощает в Хтах 410 им. [2]
Водные растворы реагента устойчивы не менее 3 мес. [3]
Водные растворы реагента неустойчивы, особенно в кислой среде. Его применяют при комплексонометрических титрованиях в щелочной среде в виде смеси реагента с хлоридом натрия ( соотношение 1: 100) в количестве 0 2 - 0 3 г на каждое определение. [4]
Водный раствор реагента устойчив в течение нескольких месяцев, разрушается при действии минеральных кислот. При рН 1 - 11 реагент образует с ионами меди ( II) комплекс фиолетового цвета. При титровании раствором комплексона III комплекс разрушается, и в точке эквивалентности окраска раствора переходит в зеленую. Двухзарядные ионы никеля, кобальта, цинка, кадмия, свинца в аналогичных условиях образуют с реагентом ярко окрашенные комплексы. При титровании в слабокислой среде определению содержания меди не мешают большие количества алюминия и марганца. [5]
Водные растворы реагента флуоресцируют в кислой среде голубым цветом, в присутствии ионов железа и перекиси водорода свечение постепенно ослабевает вследствие окисления реагента. [6]
Водные растворы реагента бесцветны и не флуоресцируют. [7]
Водные растворы реагента окрашены в розовый цвет, в слабокислой среде арсеназо I образует комплексы фиолетового цвета. [8]
Применялся водный раствор реагента, если растворитель не оговорен особо, Реакции выполнялись па фильтровальной бумаге капельным методом. [9]
Цвет водного раствора реагента при рН 1 - 4 5-малиново-красный, при рН 4 5 - 7-фиолетово-красный, при рН 9 - 10 5 - синий. Ионы Fe3, Crv Vv и Zriv в слабокислой среде обесцвечивают растворы реагента, ионы WVI и Hgl вызывают слабое фиолетовое окрашивание, ионы Си2 дают сине-фиолетовое окрашивание. Ионы большинства других элементов не вызывают изменения окраски реагента. [10]
Цвет водного раствора реагента при рН 1 - 4 5 - малиново-красный, при рН 4 5 - 7 - фиолетово-красный, при рН 9 - 10 5 - синий. Ионы Fe3, Crvl, Vv и Zrlv в слабокислой среде обесцвечивают растворы реагента, ионы Wvl и Hgj вызывают слабое фиолетовое окрашивание, ионы Си2 дают сине-фиолетовое окрашивание. Ионы большинства других элементов не вызывают изменения окраски реагента. [11]
При приготовлении водного раствора реагента необходимо пользоваться защитными очками, резиновыми фартуками и перчатками. При высыпании сухого реагента из мешков необходимо пользоваться противо-пылевыми респираторами, очками и спецодеждой. Попавший на кожу жидкий реагент следует сразу же смыть водой, а при попадании Б глаз - промыть 2 % - ным раствором борной или уксусной кислоты, а затем водой. [12]
При взаимодействии водного раствора реагента с ионами кобальта образуются комплексные соединения красно-коричневого цвета. При рН 6 5 - 7 5 образуется при 60-кратном избытке реагента комплекс с максимумом светопоглощения при 475 ммк; окраска развивается в течение 30 мин. При рН 8 5 - 11 0 образуется при 45-кратном избытке реагента другое комплексное соединение с максимумом при 390 ммк, окраска развивается через 50 мин. Интенсивность окраски обоих комплексов постоянна во времени и не изменяется 10 час. [13]
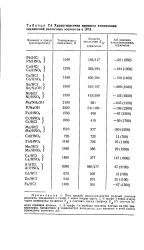 |
Характеристики процесса атомизации соединений различных элементов в ЭТА. [14] |
Под средой подразумевается водный раствор реагента, указанного в графе 1 через косую черту. [15]
Страницы: 1 2 3 4