Чистый водный раствор
Cтраница 2
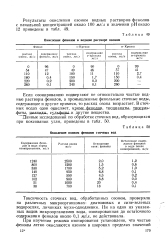 |
Окисление фенолов в водном растворе озоном.| Окисление озоном фенолов сточных вод. [16] |
Если озонированию подвергают не относительно чистые водные растворы фенолов, а промышленные фенольные сточные воды, содержащие и другие примеси, то расход озона возрастает. В сточных водах одон одисляет, кроме фенодпл, тиоцдадазы, тиосуль-фаты, цианиды, сульфиды. [17]
QH 0 737 в чистом водном растворе снижаются до § н 0 497 и о н 0 475 в растворе с 99 мол. [18]
 |
Температуры кипения азеотропных смесей этиленхлоргидрина. [19] |
Азеотропная смесь, отогнанная из чистого водного раствора при 400 мм давления, содержит 40 5 % по весу зтиленхлоргидрина, в то время как постоянно-кипящая смесь, полученная из насыщенного солевого раствора при том же давлении, содержит 57 8 % хлоргидрина. [20]
Рост кристаллов галогенидов щелочных металлов из чистых водных растворов очень затруднен. Но присутствие 0 1 % H2S04 0 1 % Pb ( N03) 2 сильно снижает скорость роста и дает возможность вырастить прозрачные совершенные кристаллы большого размера [ Buckley, 1951, стр. Этот способ применяется и в промышленности, хотя в этом случае кристаллы захватывают до 270 ррт свинца. [21]
Эта попытка, хорошо удавшаяся на чистых водных растворах перекиси водорода, оказалась, к сожалению, неприменимой для анализа реакционных смесей, так как титрование растягивалось во времени и, кроме того, давало заниженные результат. [22]
Иодноватокислый калий и является конечным продуктом электролиза чистого водного раствора йодистого калия. [23]
Сульфид аммония обычно готовят в лаборатории путем насыщения судебнохимически чистого водного раствора аммиака очищенным от мышьяка сероводородом. [24]
Для характеристики атомно-абсорбцион-ного прибора пределы обнаружения измеряются по чистым водным растворам каждого элемента и по наиболее сильным его линиям. [25]
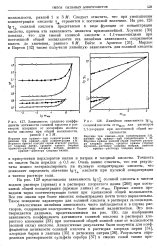 |
Зависимость среднего коэффициента активности соляной кислоты в растворах хлоридов от логарифма моляльности кислоты при общей моляльности. [26] |
На рис. 129 представлена зависимость Igyi соляной кислоты в чистом водном растворе ( кривая) и в растворах хлористого цезия [266] при постоянной общей концентрации ( прямые линии) от mHci - Прямые линии проведены через соответствующие точки при одинаковой общей моляльности. Все эти линии при более высоких концентрациях почти точно параллельны. Такое поведение характерно для соляной кислоты в растворах галогенидов. [27]
На рис. 129 представлена зависимость lgy соляной кислоты в чистом водном растворе ( кривая) и в растворах хлористого цезия [266] при постоянной общей концентрации ( прямые линии) от тцс. Прямые линии проведены через соответствующие точки при одинаковой общей моляльности. Все эти линии при более высоких концентрациях почти точно параллельны. Такое поведение характерно для соляной кислоты в растворах галогенидов. [28]
Если исследуется экстракция довольно хорошо ионизирующей кислоты или основания из чистых водных растворов, то при вычислениях учитывают степень их ионизации. [29]
Оно утверждает равенство друг другу коэффициентов активности ионов КС1 в чистых водных растворах при любой данной концентрации соли. Далее предполагается, что коэффициенты активности К и С1 - имеют те же значения и в других смесях с теми же ионной силой и концентрациями обоих ионов. Тогда коэффициент активности С1 - рассматривается как одна и та же величина в следующих растворах: 0 1 М НС1, смесь 0 01 М НС1 и 0 09 М КС1 и в 0 1 М NaCl. Эта величина принимается в каждом случае равной среднему коэффициенту активности КС1 в его 0 1 М растворе. [30]
Страницы: 1 2 3 4