Насыщенный раствор - вещество
Cтраница 2
Каждой температуре соответствует определенная растворимость данного вещества. Если охладить насыщенный раствор вещества, растворимость которого с температурой повышается, то растворенное вещество выпадает в осадок в таком количестве, что раствор остается насыщенным при той температуре, до которой он охлажден. Однако в некоторых случаях при медленном охлаждении растворенное вещество не выделяется. Тогда говорят, что раствор пересыщен. Но это очень неустойчивое состояние раствора; достаточно какому-нибудь кристаллику или пылинке попасть в раствор, чтобы избыток соли выпал в осадок. [16]
К слеживанию склонны гигроскопичные соли, растворимость которых сильно меняется при изменении температуры. Гигроскопичность зависит от давления водяного пара над насыщенным раствором вещества. Чем меньше давление пара над раствором, тем выше его гигроскопичность: если давление водяного пара в воздухе выше, чем давление его над насыщенным раствором, удобрение поглощает влагу из воздуха. [17]
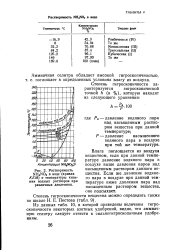 |
Растворимость NH4N03 в воде ( кривая КЕМ и температуры кипения водных растворов при различных давлениях. [18] |
Влага поглощается из воздуха веществом, если при данной температуре давление водяного пара в воздухе выше давления паров над насыщенным раствором данного вещества. Если же давление водяного пара в воздухе при данной температуре ниже давления пара над насыщенным раствором вещества, оно подсыхает. [19]
В / юльшинстве случаев промывка производится путем вытеснения маточной жидкости ( фильтрата) из слоя осадка водой. Для растворимых в воде осадков в качестве промывной жидкости применяют разбавленные растворы солей и кислот ( поваренной соли, хлористого калия, серной кислоты и др.), а иногда - насыщенный раствор вещества, из которого состоит осадок. [20]
В большинстве случаев промывка производится путем вытеснения водой маточной жидкости ( фильтрата) из слоя осадка. Для обработки растворимых в воде осадков в качестве промывной жидкости применяют разбавленные растворы солей и кислот ( поваренной соли, хлористого калия, серной кислоты и др.), а иногда - насыщенный раствор вещества, из которого состоит осадок. [21]
На различной растворимости твердых веществ при различных температурах основан метод очистки политермической кристаллизацией. Готовят насыщенный раствор вещества при высокой температуре, а затем раствор охлаждают. [22]
При низкой растворимости влияние загрязнений неводной системы следами воды может быть значительным. Более того, следует отметить, что надежные значения растворимости трудно получить даже для воды. Тем не менее, если рассматривать насыщенные растворы вещества в воде и в каком-либо другом растворителе и если можно показать, что каждый раствор находится в равновесии с тем же твердым веществом, то величина у определяется соотношением произведений растворимости ( / Csp) водн. Для гипотетического случая совершенно несмешивающихся растворителей относительный коэффициент активности переноса растворенного вещества равен коэффициенту распределения вещества между двумя растворителями. [23]
Он основан на разной растворимости компонентов смеси. Процесс кристаллизации включает в себя: 1) приготовление нагретого насыщенного раствора вещества в подходящем растворителе; 2) фильтрование горячего раствора от нерастворившихся примесей; 3) охлаждение раствора, вызывающее кристаллизацию; 4) отделение кристаллов от маточного раствора; 5) сушку кристаллов. [24]
Рассмотрим классические представления, касающиеся диффузионной кинетики реакций между жидким раствором и твердым телом. Теория этого вопроса на примере растворения твердых тел в жидкостях разработана первоначально Нерястом. Согласно теории Нернета в слое жидкости у самой поверхности твердого тела возникает насыщенный раствор вещества. Растворение идет путем диффузии вещества из этого слоя в объем раствора. [25]
Гигроскопичность ( способность вещества к адсорбции влаги из воздуха) обычно определяется относительной влажностью воздуха над насыщенным раствором данного водорастворимого вещества, или гигроскопической точкой. Вещество адсорбирует влагу в том случае, когда давление водяных паров в окружающем воздухе при данной температуре выше давления паров над насыщенным раствором данного вещества. И наоборот, вещество подсыхает, если давление водяных паров в воздухе при данной температуре ниже давления их над насыщенным раствором вещества. [26]
Поэтому формула I должна быть отвергнута. Кроме того, против нее свидетельствует также слишком высокая для дизамещенного винилового эфира температура плавления ( 153 - 156 С) и плохая растворимость в обычных органических растворителях. Наличие интенсивной полосы поглощения в ИК-спектре кристаллического образца ( паста с вазелиновым маслом) при 1570 см 1 и интенсивной полосы поглощения при 1620 смг1 для насыщенного раствора вещества в ацетонитриле, которые можно отнести к хелатному карбонилу [9], позволяют предположить, что более вероятным является строение II, так как оно допускает возникновение хелатного карбонила вследствие возможности кето-енольной и кольчато-цепной таутомерии и образование прочных внутримолекулярных водородных связей. Кроме того, в ИК-спектре кристаллического образца обнаружены полосы поглощения при 1170 см 1 ( колебания эфирной С - 0-группы) и 1006 см-1 ( колебания С - ОН) и малоинтенсивные полосы при 1642 и 1658 см 1, которые можно отнести к валентным колебаниям двойной связи. [27]
Страницы: 1 2