Анализируемый раствор - наносенок
Cтраница 2
Некоторые исследователи вводят растворы в зону разряда на поверхности нижнего электрода, имеющего форму пластинки [166] или желобка [167] и движущегося в горизонтальной плоскости. Анализируемый раствор наносят на электрод, выпаривают и сухой остаток анализируют в дуге или искре. [16]
Обычно анализ начинают с испытания реакции среды и определения рН раствора. Для этого каплю анализируемого раствора наносят стеклянной палочкой на индикаторную бумагу или помещают каплю индикатора в исследуемый раствор ( см. гл. [17]
Метод кольцевой печи предназначен для анализа одной капли раствора, содержащего несколько ионов. Метод сводится к следующему: фильтровальную бумагу помещают на нагревательный круг электрической печи и каплю анализируемого раствора наносят в центр бумаги. Благодаря быстрому выпариванию промывной жидкости ( чему способствует горячая поверхность) вымываемые ионы концентрируются в виде кольца. [18]
Метод кольцевой печи предназначен для анализа одной капли раствора, содержащего несколько ионов. Метод сводится к следующему: фильтровальную бумагу помещают на нагревательный круг электрической печи и каплю анализируемого раствора наносят в центр бумаги. Добавление реагента фиксирует положение отдель - - ных ионов, в то время как другие ионы смещаются к периферии кольца вследствие капиллярной активности фильтровальной бумаги. Благодаря быстрому выпариванию промывной жидкости ( чему способствует горячая поверхность) вымываемые ионы концентрируются в виде кольца. [19]
 |
Схема лампы с полым Катодом. [20] |
В другом варианте атомно-абсорбционного анализа вещество в атомарное состояние переводят в графитовой кювете ( рис. XII. Она представляет собой графитовую трубку, внутренний диаметр которой 3 - 5 мм, снабженную мощным электрическим нагревателем; последний обеспечивает нагревание до - 2000 К. Анализируемый раствор наносят и сушат на поверхности угольного электрода, предварительно покрытого раствором полистирола. [21]
Через 24 часа суспензию отфильтровывают. Фильтратом пропитывают фильтровальную бумагу и затем высушивают ее. Каплю анализируемого раствора наносят на приготовленную описанным выше способом фильтровальную бумагу: образуется красное пятно. [22]
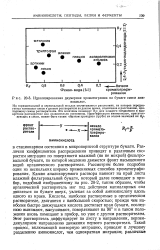 |
Идеализированная двумерная хроматограмма на бумаге смеси аминокислот. [23] |
Различия коэффициентов распределения приводят к различным скоростям миграции по поверхности влажной ( но не мокрой) фильтровальной бумаги, по которой медленно движется фронт насыщенного водой органического растворителя. Рассмотрим более подробно один из нескольких широко применяемых способов хроматографи-рования. Каплю анализируемого раствора наносят на край листа влажной фильтровальной бумаги, который далее помещают в прибор, подобный изображенному на рис. 20 - 2, таким образом, чтобы органический растворитель мог под действием капиллярных сил двигаться по бумаге вверх, увлекая за собой аминокислоту вдоль одного из краев. Кислоты, наиболее растворимые в органическом растворителе, двигаются с наибольшей скоростью; прежде чем наиболее быстро движущаяся кислота достигает края бумаги, последнюю вынимают, высушивают, поворачивают на 90 и в таком положении вновь помещают в прибор, но уже с другим растворителем. Этот растворитель диффундирует по листу в направлении, перпендикулярном направлению движения первого растворителя. [24]
Для разделения веществ методом хроматографии в тонком слое сорбента используют хроматогра-фические камеры подходящего размера. На дно камеры наливают подвижную фазу в количестве, достаточном для образования слоя глубиной 0 5 см, камеру закрывают и выдерживают для насыщения парами растворителей 30 - 60 мин. Стен - ки камеры для полноты насыщения мождо обкладывать фильтровальной бумагой. Анализируемый раствор наносят микропипеткой или микрошприцем на линию старта, проведенную на расстоянии 2 - 3 см от нижнего края пластинки, так, чтобы пятна образцов отстояли друг от друга и от краев слоя сорбента не менее чем на 2 см. Нежелательное растекание пятен анализируемых проб при нанесении предотвращают путем периодического подсушивания. [25]
Для разделения веществ методом хроматографии в тонком слое сорбента используют хроматографические камеры подходящегс размера. На дно камеры наливают подвижную фазу в количестве, достаточном для образования слоя глубиной 0 5 см, камеру закрывают и выдерживают для насыщения парами растворителей 30 - 60 мин. Анализируемый раствор наносят микропипеткой или микрошприцем на линию старта, проведенную на расстоянии 2 - 3 см от нижнего края пластинки, так, чтобы пятна образцов отстояли друг от друга от краев слоя сорбента не менее чем на 2 см. Нежелательное растекание пятен анализируемых проб при нанесении предотвращают путем периодического подсушивания. [26]
Смесь адсорбента со связующим наносят на подложку в виде тонкой суспензии и избыточный растворитель удаляют. Это делают очень мягким свинцовым карандашом, стараясь не повредить слой адсорбента в точке нанесения пробы, поскольку это может привести к деформации пятен. При нанесении линии финиша целесообразно прорезать слой адсорбента до подложки таким образом, чтобы в слое образовалась хорошо заметная щель. Когда растворитель достигает финишной линии, прочерченной таким образом, проявление автоматически прекращается. Анализируемый раствор наносят на линию старта с помощью микропипетки и помещают пластинку в герметичный контейнер, на дно которого налит слой растворителя толщиной около 0 5 см. Растворитель поднимается по пластинке под действием капиллярных сил, пока не достигнет линии финиша, после чего пластинку извлекают из контейнера, дают растворителю испариться и устанавливают местоположение пятен различных соединений каким-либо методом, позволяющим сделать бесцветные пятна видимыми. Для этой цели применяют самые разные реактивы. Последняя величина измеряется расстоянием между стартовой линией и фронтом растворителя. [27]
Нингидрин находит широкое применение при двух хроматографических методах анализа аминокислот. Одним из них является хроматография на бумаге; в этом методе разделение аминокислот происходит вследствие различия коэффициентов распределения между водой и органическим растворителем. Водная фаза удерживается в стационарном состоянии в микропористой структуре бумаги. Различия коэффициентов распределения приводят к различным скоростям миграции по поверхности влажной ( но не мокрой) фильтровальной бумаги, по которой медленно движется фронт насыщенного водой органического растворителя. Рассмотрим более подробно один из нескольких широко применяемых способов хроматографирования. Каплю анализируемого раствора наносят на край листа влажной фильтровальной бумаги, который далее помещают в прибор, подобный изображенному на рис. 20 - 2, таким образом, чтобы органический растворитель мог под действием капиллярных сил двигаться по бумаге вверх, увлекая за собой аминокислоту вдоль одного из краев. [28]
Страницы: 1 2