Анализируемый раствор - проба
Cтраница 2
В работе [107] описан применимый для непосредственного определения как свободных, так и связанных жирных кислот метод этерификации и переэтерификации, в котором анализ ведут путем обработки раствора пробы в хлороформе раствором едкого натра и метилата натрия - 3Н в метаноле - 3Н5 взятом в объеме, равном объему анализируемого раствора пробы. Для того чтобы замедлить разложение полученного раствора, его хранят в полиэтиленовом сосуде на холоду; кроме того, необходимо предохранять этот раствор от контакта с воздухом, поскольку под действием воздуха в течение 4 ч в реагенте образовывалось большое количество производных. Для проведения анализа сухую пробу растворяют в 0 1 - 1 мл хлороформа и добавляют в полученный раствор такой же объем реагента. Затем сосуд с раствором плотно закрывают пробкой и встряхивают в течение 1 ч при комнатной температуре. Сразу же по окончании встряхивания к раствору в сосуде добавляют 1 каплю раствора фенолфталеина в абсолютном метаноле и нейтрализуют его ледяной уксусной кислотой. После этого полученный раствор количественно ( смывая хлороформом) переносят в делительную воронку и дважды промывают десятикратным избытком ( по объему) дистиллированной воды; для определения менее 1 мкМ кислоты рекомендуется провести еще одно дополнительное промывание. Хлороформную фазу переносят из воронки в другой сосуд и испаряют растворитель под вакуумом. К полученному остатку добавляют метанол, затем вращают сосуд и выжидают испарения метанола; при определении менее 1 мкМ кислоты эту процедуру повторяют несколько раз. Для измерения радиоактивности полученного остатка его растворяют в толуольном растворе сцинтиллятора. Для того чтобы убедиться в отсутствии нелетучих радиоактивных примесей в метаноле, проводят холостой опыт. Результаты, полученные путем непосредственного измерения радиоактивности метанола, хорошо согласовывались с результатами, полученными с использованием стандартных проб кислоты. Если в пробе содержатся глицериды или другие эфиры, то перед определением свободной кислоты их следует удалять из раствора. Быстрота анализа, простота и хорошая точность результатов при определении наномольных концентраций делают этот метод весьма привлекательным для определения полного содержания жирных кислот. К положительным его чертам относятся также и используемые в нем мягкие условия этерификации и количественная переэтерификация, катализируемая едким натром. [16]
В работе [107] описан применимый для непосредственного определения как свободных, так и связанных жирных кислот метод этерификации и переэтерификации, в котором анализ ведут путем обработки раствора пробы в хлороформе раствором едкого натра и метилата натрия - 3Н в метаноле - 3Н, взятом в объеме, равном объему анализируемого раствора пробы. Для того чтобы замедлить разложение полученного раствора, его хранят в полиэтиленовом сосуде на холоду; кроме того, необходимо предохранять этот раствор от контакта с воздухом, поскольку под действием воздуха в течение 4 ч в реагенте образовывалось большое количество производных. Для проведения анализа сухую пробу растворяют в 0 1 - 1 мл хлороформа и добавляют в полученный раствор такой же объем реагента. Затем сосуд с раствором плотно закрывают пробкой и встряхивают в течение 1 ч при комнатной температуре. Сразу же по окончании встряхивания к раствору в сосуде добавляют 1 каплю раствора фенолфталеина в абсолютном метаноле и нейтрализуют его ледяной уксусной кислотой. После этого полученный раствор количественно ( смывая хлороформом) переносят в делительную воронку и дважды промывают десятикратным избытком ( по объему) дистиллированной воды; для определения менее 1 мкМ кислоты рекомендуется провести еще одно дополнительное промывание. Хлороформную фазу переносят из воронки в другой сосуд и испаряют растворитель под вакуумом. К полученному остатку добавляют метанол, затем вращают сосуд и выжидают испарения метанола; при определении менее 1 мкМ кислоты эту процедуру повторяют несколько раз. Для измерения радиоактивности полученного остатка его растворяют в толуольном растворе сцинтиллятора. Для того чтобы убедиться в отсутствии нелетучих радиоактивных примесей в метаноле, проводят холостой опыт. Результаты, полученные путем непосредственного измерения радиоактивности метанола, хорошо согласовывались с результатами, полученными с использованием стандартных проб кислоты. Если в пробе содержатся глицериды или другие эфиры, то перед определением свободной кислоты их следует удалять из раствора. Быстрота анализа, простота и хорошая точность результатов при определении наномольных концентраций делают этот метод весьма привлекательным для определения полного содержания жирных кислот. К положительным его чертам относятся также и используемые в нем мягкие условия этерификации и количественная переэтерификация, катализируемая едким натром. [17]
Фильтр с отобранной пробой помещают в пробирку, приливают пипеткой 9 9 мл воды, встряхивают, добавляют 0 1 мл соляной кислоты и перемешивают. Измеряют оптическую плотность анализируемого раствора пробы аналогично градуировочным растворам, по сравнению с контролем, который готовят одновременно и аналогично пробе. [18]
Затем растворы охлаждают, фильтруют и доводят объем до 6 мл дистиллированной водой. Измеряют оптическую плотность анализируемого раствора пробы аналогично градуировочным растворам. [19]
По 3 мл исследуемого раствора из каждого поглотительного сосуда переносят в колориметрические пробирки, добавляют по 0 1 мл раствора хлорного железа и взбалтывают. Через 15 минут оптическую плотность анализируемого раствора пробы измеряют аналогично градуировочным растворам по сравнению с контролем, который готовят аналогично пробе. [20]
Одновременно с анализируемой пробой проводят полярографи-рование двух контрольных проб с фильтрами АФА-ХА-20. Среднее значение высот пиков контрольной пробы вычитают из высоты пика анализируемого раствора пробы и проводят расчет. [21]
Устанавливают рН 3 5 ( то рН - метру) анализируемого раствора пробы, содержащего не более 1 % хлоридов, и экстрагируют серебро небольшими порциями раствора дитизона до тех пор, пока органическая фаза не будет оставаться чисто зеленой. Полученный водный раствор разбавляют до 60 мл и снова экстрагируют раствором дитизона. Экстракт фотометрируют при 462 нм. [22]
Спустя 45 мин измеряют поглощение раствора при 532 нм в 1 -сантиметровой кювете, используя воду в качестве раствора сравнения. Затем измеряют поглощение контрольного раствора, приготовленного так же, как и анализируемый раствор пробы, но не содержащего Re; полученное значение учитывают при расчете содержания Re в образце. [23]
 |
Кулонометричеокая ячейка для титрования кислот. [24] |
Как и в других кулонометрических методах анализа, раствор пробы должен хорошо перемешиваться. Ячейку можно закрыть плотной крышкой, снабженной трубкой для постоянного ввода азота или ( иногда) диоксида углерода и отверстием для вывода этих газов и удаления кислорода из анализируемого раствора пробы. [25]
Фильтр с отобранной пробой переносят в колориметрическую пробирку, заливают 6 мл 3 % - ной соляной кислоты и ставят в кипящую водяную баню на 30 минут. Затем растворы охлаждают, фильтруют и доводят объем до 6 мл 3 % - ной соляной кислоты. Оптическую плотность анализируемого раствора пробы измеряют аналогично градуировочным растворам. [26]
К 3 мл раствора пробы добавляют 1 мл раствора Na2CO3 и 9 мл этанола. Для определения флуоресценции анализируемого раствора, обусловленной загрязнениями этанола и цробы, измеряют интенсивность флуоресценции, используя раствор сульфата хинина в качестве раствора сравнения. Затем к анализируемому раствору пробы добавляют 4 мл раствора бензоина и через 10 мин измеряют флуоресценцию относительно раствора сульфата хинина. Поглощение раствора пробы до добавления реагента учитывают при расчете концентрации бора. [27]
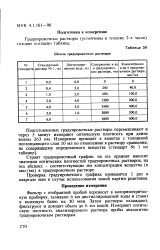 |
Шкапа градуироночных растворов. [28] |
Фильтр с отобранной пробой переносят в колориметрическую пробирку, заливают 6 мл дистиллированной воды и ставят в кипящую баню на 30 мин. Затем растворы охлаждают, фильтруют и доводят объем до 6 мл водой. Измеряют оптическую плотность анализируемого раствора пробы аналогично градуировочным растворам. [29]
Фильтр с пробой помещают в платиновую чашку, добавляют 1 мл воды, 3 мл серной кислоты, 5 мл фтороводородной кислоты и нагревают при периодическом помешивании фторопластовой палочкой на плитке слабого нагрева до образования сухого остатка. Затем в чашку приливают 5 мл воды и 5 мл хлороводородной кислоты и растворяют пробу при нагревании. Полученный раствор, отфильтровывая, количественно переносят в мерную колбу вместимостью 50 мл, доводят водой до метки и перемешивают. Анализируемые растворы проб подают в атомизатор прибора и фотометрируют аналогично градуировочным растворам. [30]
Страницы: 1 2 3