Растворение - хлористый калий
Cтраница 3
Мы знаем, что даже простое растирание соли в порошок требует затраты значительного количества энергии. Очевидно, что для разделения соли на отдельные ионы необходимо затратить еще больше энергии. Откуда же при растворении хлористого калия в воде берется такое большое количество энергии для отрыва ионов от кристалла. В основном этот процесс осуществляется за счет энергии гидратации ионов. Для хлористого калия эта энергия составляет ( см. табл. 66) примерно 81 - f - 84 165 ккал / моль и, следовательно, действительно покрывает большую часть энергии, необходимой для выделения ионов из кристалла. Остающиеся 170 - - 165 5 ккал / моль покрывают за счет энергии теплового движения, и растворение сопровождается поглощением теплоты из окружающей среды. [31]
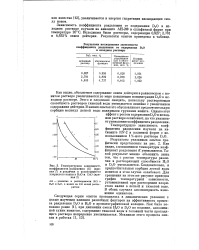 |
Температурная зависимость коэффициента разделения ( К ( крк-вая 1 и различия в растворимости хлористого калия в НаО и DjO ( кривая 2. [32] |
Как видно, с повышением температуры коэффициент разделения К уменьшается. Такой результат можно объяснить лишь тем, что с ростом температуры различия в растворяющей способности Н20 и D20 уменьшаются. Следовательно, и предпочтительная сорбция легкой воды ионитом в этом случае ослабевает. Для сравнения на этом же рисунке приведен график температурной зависимости, установленной при растворении хлористого калия в легкой и тяжелой воде. В обоих случаях закономерность изменения одинакова. [33]
Приведенная диаграмма растворимости хорошо иллюстрирует процесс получения хлористого калия. Однако в производственных условиях этот процесс несколько осложняется. Как было сказано выше, в сильвините хлористого натрия значительно больше, чем хлористого калия. По причине большей растворимости первого состав раствора характеризуется не равновесной точкой св ( при 100), а точкой е6; в процессе выщелачивания происходит растворение хлористого калия и состав раствора перемещается по линии еесв. В случае, когда раствор недонасыщен по хлористому калию и его состав характеризуется точкой /, кривой охлаждения будет линия fg, параллельная оси ординат; в момент пересечения линий fg и qc6 из раствора начнет выпадать хлористый натрий. При последующем охлаждении будет выпадать ( по кривой gmj. [34]
 |
Электропроводность хлоридов щелочных металлов. [35] |
Мы знаем, что даже простое растирание соли в порошок требует затраты значительного количества энергии. Очевидно, для разделения соли на отдельные ионы необходимо затратить много больше энергии. Для хлористого калия это количество энергии составляет 170 ккал / моль. Откуда же при растворении хлористого калия в воде берется такое большое количество энергии для отрыва ионов от кристалла. В основном этот процесс осуществляется за счет энергии гидратации ионов. Для хлористого калия эта энергия составляет ( см. табл. 37) примерно 81 84165 ккал / моль и, следовательно, действительно покрывает большую часть энергии, необходимой для выделения ионов из кристалла. Остающиеся 170 - 165 5 ккал / моль покрываются за счет энергии теплового движения и растворение сопровождается поглощением теплоты из окружающей среды. [36]
 |
Электропроводность хлоридов щелочных металлов. [37] |
Мы знаем, что даже простое растирание соли в порошок требует затраты значительного количества энергии. Очевидно, для разделения соли на отдельные ионы необходимо затратить много больше энергии. Для хлористого калия это количество энергии составляет 170 ккал / моль. Откуда же при растворении хлористого калия в воде берется такое большое количество энергии для отрыва ионов от кристалла. В основном этот процесс осуществляется за счет энергии гидратации ионов. Для хлористого калия эта энергия составляет ( см. табл. 37) примерно 81 84 165 ккал / моль и, следовательно, действительно покрывает большую часть энергии, необходимой для выделения ионов из кристалла. Остающиеся 170 - 165 5 ккал / моль покрьь ваются за счет энергии теплового движения и растворение сопровождается, поглощением теплоты из окружающей среды. [38]
Радиоактивная сера в момент образования в кристаллах, из которых не удален воздух, окисляется кислородом воздуха, который может содержаться в кристаллах хлористого калия. Кроме того, во время облучения кристаллов образуется элементарный хлор, который окисляет серу, причем образуется хлористая и полухлористая сера. Гидролиз этих соединений приводит к образованию сульфит - или сульфат-ионов. При растворении кристаллов хлористого калия, содержащих 63 % радиоактивной серы в виде сульфата, в дестиллированной воде, из которой воздух не удален, вся радиоактивная сера превращается в сульфат. В случае отсутствия носителя сера окисляется до шестивалентного состояния. При растворении хлористого калия в спирте окисления не происходит в течение недели. [39]
Страницы: 1 2 3