Растворение - олово
Cтраница 1
Растворение олова в серной кислоте длится несколько десятков часов. [1]
Растворение олова производят при слабом нагревании. Чтобы избежать окисления SnQ2, колбу закрывают пробкой, снабженной клапаном. Для этого на небольшом отрезке ( 3 - 4 см) тонкостенной резиновой трубки делают продольный надрез. Один конец резиновой трубки закрывают кусочком стеклянной палочки, а другой соединяют со стеклянной трубкой, проходящей через пробку колбы. [2]
Растворение олова в серной кислоте длится несколько десятков часов. [3]
Растворение олова ведется при температуре 60 - 70 и плотности тока 1 а / дм. В качестве катодов используют железные листы, на которых олово осаждается в виде губчатой массы. [4]
Растворение олова в этом составе основано на реакции контактного вытеснения сурьмы оловом, которая защищает металл основы от взаимодействия с соляной кислотой. Осадок сурьмы затем удаляют в растворе едкого натра. [5]
Растворение олова в этом составе основано на реакции контактного вытеснения олова сурьмой, которая защищает металл основы от взаимодействия с соляной кислотой. Осадок сурьмы затем удаляют в растворе едкого натра. [6]
После растворения олова в кодбу добавляют еще 50 мл НС1 уд. [7]
После растворения олова потенциал электрода начнет расти, подымется до потенциала СшЗп, и его кристаллы начнут растворяться, диссоциируя в дальнейшем на ионы меди и олова. [8]
После растворения олова объем доводят до 10 мл дистиллированной водой. [9]
После растворения олова и охлаждения жидкости добавляют по каплям при взбалтывании 2 5 мл 10 % - ного раствора медного купороса, доводят водой до метки и взбалтывают. Реактив годен только в течение 10 часов, по-этбму употреблять его следует всегда свежеприготовленным. [10]
При растворении олова в концентрированных щелочах образуются станниты - соли полимерной оло-вянистой кислоты, а в присутствии окислителей - стан-наты, или соли оловянной кислоты. В водных растворах эти соли гидролизуются и конденсируются, выделяя воду. При этом образуется высокополимерный анион гидрата окиси олова mH2O - nSnO, называемый а-оловянной кислотой. При стоянии он продолжает конденсироваться в высокоупорядоченное кристаллическое полимерное тело - р-оловянную кислоту, плохо растворимую в кислотах и щелочах. Это происходит следующим образом. Щелочь разрывает связи Sn-О - Sn в решетке и образуются концевые и функциональные NaO-группы; при растворении в кислоте катионы этих групп заменяются протонами, и вещество приобретает строение а-оловянной кислоты. [11]
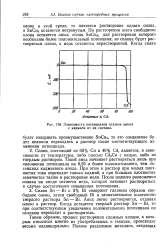 |
Зависимость потенциалов сплавов цинка с кадмием от их состава. [12] |
По растворении всего свободного олова останется лишь сплав SnCua, для растворения которого необходим более положительный потенциал; из сплава будет растворяться олово, а медь останется нерастворенной. [13]
Возможно ли растворение олова в воде. [14]
Диффузионный процесс растворения олова представляется нам движением частиц к поверхности диска и продуктов реакции от него через газовую вуаль, а также через изъяны в ней. В результате блокирования олова газовой вуалью величина поверхности, доступная для реакции, видимо, во много раз меньше поверхности диска. [15]
Страницы: 1 2 3 4