Растворение - спирт
Cтраница 3
Механизм [37], лучше всего связывающий между собой и объясняющий многочисленные примеры бензиловой перегруппировки, предполагает, что вначале происходит быстрое и обратимое присоединение иона гидроксила к одной из карбонильных групп, за которым следует миграция арила к относительно бедному электронами соседнему атому углерода [ уравнение ( 7) ]; эта миграция является стадией, лимитирующей общую скорость процесса. Быстрый перенос протона, приводящий к конечному продукту, происходит обычно при растворении спиртов или карбоновых кислот в гидроксилсодержащих растворителях. [31]
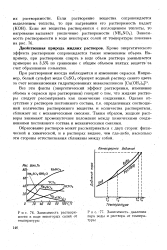 |
Зависимость растворимости в воде некоторых солей от температуры. [32] |
Кроме энергетического эффекта растворение сопровождается также изменением объема. Например, при растворении спирта в воде объем раствора уменьшается примерно на 3 5 % по сравнению с общим объемом взятых веществ за счет образования сольватов. [33]
Ряд свойств растворов ( плотность, теплоемкость и др.) не являются аддитивными - они не могут быть вычислены из соответствующих свойств чистых компонентов раствора. Например, при смешивании 500 мл этилового спирта и 500 мл воды образующийся раствор имеет объем не 1000 мл, а 965 мл. Следовательно, при растворении спирта в воде происходит сжатие системы. Это явление носит название контракции ( лат. Однако известны случаи, когда суммарный объем раствора больше суммы объемов растворяемого вещества. [34]
Кроме энергетического эффекта растворение сопровождается также изменением объема. Например, при растворении спирта в воде объем раствора уменьшается примерно на 3 5 % по сравнению с общим объемом взятых веществ за счет образования сольватов. [35]
Кроме энергетического эффекта растворение сопровождается также изменением объема. Например, при растворении спирта в воде объем раствора уменьшается примерно на 3 5 6 по сравнению с общим объемом взятых веществ за счет образования сольватов. [36]
Ряд свойств растворов ( плотность, удельная теплоемкость и др.) не являются аддитивными - они не могут быть вычислены из соответствующих свойств чистых компонентов раствора. Например, при смешивании 500 мл этилового спирта и 500 мл воды образующийся раствор имеет объем не 1000 мл, а 940 мл. Следовательно, при растворении спирта в воде происходит сжатие системы. Это явление носит название контракции ( лат. Однако известны случаи, когда суммарный объем раствора больше суммы объемов растворяемого вещества. [37]
 |
Форма кристаллов. [38] |
В воде могут растворяться также жидкости и газы. При смешении жидкостей с водой возможны три случая: полная растворимость, ограниченная растворимость и практическая нерастворимость жидкости. К первому случаю относится растворение спирта в воде. Они смешиваются в любых отношениях и всегда дают однородный прозрачный раствор. Большинство жидкостей, однако, ограниченно растворяются друг в друге. Если смешать серный эфир с водой и дать смеси отстояться, получатся два слоя: верхний - насыщенный раствор воды в эфире и нижний - насыщенный раствор эфира в воде. Повышение температуры увеличивает взаимную растворимость жидкостей, и при определенной температуре они станут смешиваться в любых отношениях, граница между ними исчезнет. Такая температура называется критической. [39]
 |
Форма кристаллов. [40] |
В воде могут растворяться также жидкости и газы. При смешении жидкостей с водой возможны три случая: полная растворимость, ограниченная растворимость и практическая нерастворимость жидкости. К первому случаю относится растворение спирта в воде, которые смешиваются в любых отношениях и всегда дают однородный прозрачный раствор. Большинство жидкостей, однако, ограниченно растворяются друг в друге. Если смешать серный эфир с водой и дать смеси отстояться, получатся два слоя: верхний - насыщенный раствор воды в эфире и нижний - насыщенный раствор эфира в воде. Повышение температуры увеличивает взаимную растворимость жидкостей, и при определенной температуре они станут смешиваться в любых отношениях, граница между ними исчезнет. Такая температура называется критической. [41]
Ацетильные группы отщепляют 2 N NaOH при 20 в атмосфере водорода. Спустя час точно нейтрализуют серной кислотой. После отгонки необходимых для растворения спирта и эфира трпгаллоилацетонглюкоза частично выделяется в виде масла. Остальная часть выщелачивается уксусным эфиром. [42]
 |
Коэффициенты полярности сорбатов по системе Роршнайдера. [43] |
Как правило, авторы предлагаемых систем выбирают сорбаты-тесты, каждый из которых характеризуется одним, превалирующим видом взаимодействия. Например, считается, что основным видом специфического взаимодействия для спиртов служит водородная связь. Однако мольная свободная энергия растворения спиртов характеризует как энергию межмолекулярных сил, так и энтропию. Утверждать, что энтропия описывает какое-либо специфическое взаимодействие, было бы ошибочным. [44]
На примере линолевой, линоленовой и арахидоновой кислот исследовали влияние агрегации и добавок радикальных ловушек на процесс радиационного перекисного окисления в растворах мыл жирных кислот. Зависимость выхода гидроперекисей от концентрации мыла в системе и выход продуктов в смешанных системах свидетельствуют о том, что конфигурация ненасыщенных фрагментов играет существенную роль при определении длины цепи реакции перекисного окисления. На основании ряда экспериментов по конкурентному ингибированию и по влиянию добавок S20 - показано, что основным радикалом, приводящим к инициированию цепей в данной системе, является ОН-ради-кал. Растворение спиртов, в особенности яреи-бутанола, в образованных мылом агрегатах приводит к незначительному снижению выхода сопряженных диенов, откуда следует, что радикалы спиртов в мицеллярной псевдофазе могут сами инициировать процесс перекисного окисления. Облучение растворов мыла ( Ь Ю М), содержащих низкие концентрации а-токоферола ( 2 5 10 - 6М), может привести к потере антиоксидантных и возникновению у токоферола прооксидантных свойств. [45]
Страницы: 1 2 3