Анодное растворение
Cтраница 4
Продолжение анодного растворения в трещине необходимо для роста трещины, вызванной водородом, проникающим в сталь. [46]
 |
Схема электрохонингова-ния цилиндра. [47] |
Продукты анодного растворения удаляются с обрабатываемой поверхности заготовки брусками за счет вращательного и возвратно-поступательного движений хонинговалыюй головки. Для более активного удаления продуктов анодного растворения в электролит добавляют абразивные материалы. [48]
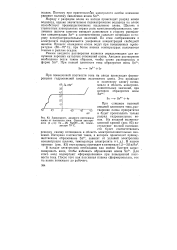 |
Зависимость анодного потенциала олова от плотности тока. Состав электролита ( в г / л. Sn - 28, NaOH - 13. температура 70 С. [49] |
Режим анодного растворения является определяющим для получения хороших катодных отложений олова. [50]
Механизм анодного растворения значительно усложняется, когда в реакции участвуют не один, а два или более сортов ионов. Так, в анодном процессе растворения железного электрода в серной кислоте принимают участие не только анионы кислоты, но и ионы гидроксила. [51]
Реакция анодного растворения протекает с участием дырок и электронов, поскольку захват электронов может происходить как из зоны проводимости, так и из валентной зоны полупроводника. Все внешние воздействия, способствующие увеличению концентрации дырок на поверхности, - нагрев, освещение, инжекция дырок через р-п-переход - ускоряют процесс анодного растворения. [52]
Продолжительность анодного растворения устанавливают в зависимости от площади и требуемой толщины слоя растворяемого покрытия. После электролиза образец вынимают из электролита, снимают осадок, взвешивают и погружают во вновь налитый электролит. Если поверхностный слой электролитически не растворяется, образец переносят в платиновый тигель, содержащий 10 мл плавиковой кислоты и одну каплю HNO3 ( 1 4) я проводят химическое растворение в течение минуты. Затем образец вынимают, промывают, взвешивают и для растворения последующего слоя погружают в электролитическую ванну. Если снова не происходит электролитического растворения покрытия, то опять - применяют химическое растворение. Эти операции повторяют до тех пор, пока последующие слои покрытия не будут анодно растворяться. Электролитическое послойное растворение образцов ведут до растворения всего покрытия и заканчивают растворением одного-двух слоев ниобиевого сплава. [53]
Процесс анодного растворения, как показал В. Н. Гусев в 1928 г., можно значительно интенсифицировать, если применять высокие плотности тока ( до 100 А / см2 и выше) и интенсивно удалять продукты анодного растворения - гидраты оксида и закиси металлов. Различают следующие разновидности ЭХРО. [54]
Условия анодного растворения в активном режиме соблюдаются в большинстве случаев лишь для небольшого диапазона значений положительного потенциала растворяющегося металла. Уже при относительно малом перенапряжении начинаются параллельно побочные процессы, например образование окислов [179], поскольку равновесные потенциалы растворения и окисления многих металлов близки по величине между собой. [55]
Страницы: 1 2 3 4