Анодное растворение - серебро
Cтраница 1
Анодное растворение серебра в кислых растворах протекает со 100 % - ной эффективностью в широком интервале плотностей тока. [1]
При анодном растворении серебра в цианистом калии возможно и растворение меди или медного подслоя деталей. По - этому после использования электролита находящееся в нем серебро может быть извлечено в виде AgCl путем осторожного подкисления электролита малыми дозами НС1 в вытяжном шкафу. Ввиду высокой опасности указанной операции ее выполнение может быть поручено только квалифицированным исполнителям. [2]
 |
Хлорсеребряный электрод. [3] |
В результате анодного растворения серебра на поверхности электрода образуется осадок AgCl. Одновременно происходит выделение газообразного хлора, который частично остается в адсорбированном состоянии на поверхности электрода. Для удаления следов хлора электрод со свежеобразованным осадком AgCl необходимо подвергнуть катодной поляризации в том же самом сосуде, но с новой порцией раствора НС1, соединив его с отрицательным полюсом аккумулятора. Электролиз ведется также в течение 15 мин. [4]
В результате анодного растворения серебра на поверхности электрода образуется осадок AgCl. Одновременно происходит выделение газообразного хлора, который частично остается в адсорбированном состоянии на поверхности электрода. Для удаления следов хлора электрод со свежеобразованным осадком AgCl необходимо подвергнуть катодной поляризации в том же самом сосуде, нос новой порцией раствора НС1, соединив его с отрицательным полюсом аккумулятора. Электролиз ведется также в течение 15 мин. [5]
Из платиноидов при анодном растворении серебра в раствор может переходить в некотором количестве палладий, его стандартный потенциал равен 0 987 в. [6]
Предложенный электролитический метод, основанный на анодном растворении серебра, обеспечивает быстрое получение желаемых концентраций металла, позволяет вести точную дозировку и регулирование процесса при помощи электроизмерительных приборов. [7]
При взаимодействии с расплавленным AgCl при 800 было обнаружено анодное растворение серебра из сплава с 12 ат. [8]
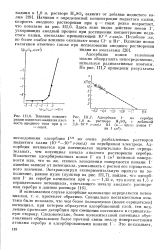 |
Йлияние концент - [ IMAGE ] 111 7. Адсорбция I на серебре. [9] |
Адсорбция начинается при потенциалах значительно более отрицательных, чем потенциал начала анодного растворения серебра. Количество адсорбированных ионов 1 - на 1 см2 истинной поверхности или, что то же, степень заполнения поверхности ионами I линейно зависит от потенциала, уменьшаясь с ростом его отрицательного значения. [10]
Деспич и Бокрис [83] предположили, что ими обнаружен безактивацион-ный процесс при катодном выделении и анодном растворении серебра. Они обосновывают это тенденцией к появлению предельного анодного и катодного токов и полной симметрией анодной и катодноц поляризационных кривых. [11]
 |
Поляризационные кривые при электроосаждении серебра из различных цианидных растворов. [12] |
Для предотвращения пассивирования серебряных анодов рекомендуется добавлять к раствору дицианоаргентата калия ( в отсутствие свободного цианида) роданид калия или аммония, которые и влияют в основном на анодное растворение серебра; влияние других компонентов электролита незначительно. [13]
Для предотвращения пассивирования серебряных анодов [19, 20] рекомендуется добавлять к раствору дицианоаргентата калия ( в отсутствие свободного цианида) роданистый калий или роданистый аммоний, которые и обусловливают в основном анодное растворение серебра; влияние других компонентов электролита незначительно. [14]
Серебро легко растворяется в азотной кислоте, слабо - в серной и практически нерастворимо в соляной кислоте и в щелочах. Анодное растворение серебра в цианистых растворах протекает беспрепятственно, что используется для его электрополирования. Серебро легко полируется и в полированном состоянии обладает хорошей отражательной способностью. [15]
Страницы: 1 2 3