Анодное растворение - титан
Cтраница 1
Анодное растворение титана в этом случае происходит не по всей поверхности электрода, а в отдельных местах. [1]
Поскольку анодное растворение титана сопровождается разрядом ионов водорода, особенно вблизи стационарного потенциала, то при активном анодном растворении будет происходить образование гидридных связей титана и торможение анодного растворения за счет гидридных связей. [2]
Поскольку анодное растворение титана сопровождается paas - рядом ионов водорода, особенно вблизи стационарного потенциала, то при активном анодном растворении будет происходить образование гидридных связей титана и торможение анодного растворения за счет гидридных связей. [3]
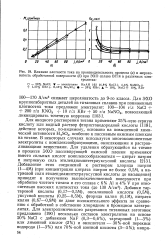 |
Влияние плотности тока на производительность процесса ( а и шероховатость обработанной поверхности ( б при ЭХО сплава ВТ14 в различных электролитах. [4] |
Для анодного растворения титана применяют 25 % - ную серную кислоту или водный раствор фтористоводородной кислоты [118], действие которых, по-видимому, основано на повышенной химической активности H2SO4, особенно к пассивным окисным пленкам на титане. В некоторых случаях использутся многокомпонентные электролиты с комплексообразующими, окисляющими и растравливающими веществами. [5]
 |
Схема развития трещины Г261. 264 ]. [6] |
Реакции анодного растворения титана не приведены. [7]
При анодном растворении титана и его сплавов с понижением плотности тока возрастает вероятность появления питтингов. При плотности тока выше 15 А / см2 этого не наблюдается. [8]
Показано, что при наложении переменного тока интенсифицируется процесс анодного растворения титана и тем в большей степени, чем выше частота наложенного переменного тока. [9]
Таким образом, следует заключить, что под действием переменного тока интенсифицируется процесс анодного растворения титана и тем в большей степени, чем выше частота наложенного переменного тока. Это связано с тем, что при наложении переменного тока в катодный полупериод происходит активация поверхности титана. В следующий затем анодный полупериод активная поверхность металла начинает растворяться, а к концу полупериода может снова пассивироваться. [10]
При смещении потенциала активного титана от стационарного значения в положительную сторону до потенциала У скорость анодного растворения титана в неокислительной кислоте возрастает вследствие облегчения протекания анодного процесса. На поверхности титана после коррозии его в этой области потенциалов электронографическим анализом обнаруживается гидрид титана. [11]
Кислоты во многом определяют значения максимальной достигнутой плотности тока, потенциала пассивации, а также дальнейший ход анодного растворения титана. [12]
Тройные сплавы титан-палладий-молибден, а также титан-палладий-хром обладают большей устойчивостью, чем двойной сплав титан-палладий, что связано с уменьшением тока анодного растворения титана вблизи потенциала полной пассивации при легировании его молибденом или хромом. [13]
Обязательно ставят глухой опыт, проводя его со всеми реактивами через весь ход анализа, начиная от нагревания смеси кислот после анодного растворения титана. [14]
Облегчение самопроизвольной пассивации легированного титана достигается за счет существенного облегчения катодной реакции выделения водорода на сплавах по сравнению с титаном, а в некоторых случаях и за счет затруднения анодного растворения титана. [15]
Страницы: 1 2 3