Растворимость - борная кислота
Cтраница 1
Растворимость борной кислоты при 0 - 2 г в 100 мл дистиллированной воды; при 20 - 5 г и при 100 - 40 г. Для получения перекристаллизованной борной кислоты в достаточном для приготовления стандартного раствора количестве следует отвесить на технических весах 10 - 12 г борной кислоты, растворить при нагревании и постоянном помешивании в 100 мл дистиллированной воды. [1]
Растворимость борной кислоты Н3ВО3 в воде при 13 С равна 38 5 г на I л раствора и 49 1 г на 20 С. [2]
Растворимость борной кислоты Н3ВО3 в воде при 13 С равна 38 5 г в 1 л раствора и 49 1 г при 20 С. [3]
Растворимость борной кислоты в присутствии моно-кальцийфосфата изучена в пределах концентраций СаО от 0 до 4.4 % в растворе; Н3В03 во всех пробах была в твердой фазе. Полученные результаты приведены в таблице. [4]
Растворимость борной кислоты Н3ВО3 в воде при 13 С равна 38 5 г в 1 л раствора и 49 1 г при 20 С. [5]
Увеличение растворимости борной кислоты с повышением тем-пературы до 25 свидетельствует о том, что наиболее благоприятными условиями для получения растворов, богатых содержанием борной кислоты, будут являться более высокие температуры. [6]
Данных о растворимости борной кислоты в присутствии фосфатов магния в литературе пет. [7]
Так как растворимость борной кислоты с повышением температуры сильно повышается ( при 0 С-1947 г, при 20 С - 39 92 г, при 102 С - насыщенный раствор - 291 2 г в 1 л), то при охлаждении она выделяется в виде характерных кристаллов. [8]
Снижение концентрации сульфата магния увеличивает растворимость борной кислоты и содержание ее в маточнике, а повышение концентрации MgSO4 снижает растворимость борной кислоты. Очистку борной кислоты производят перекристаллизацией из воды при 85 - 90J в присутствии активированного угля. Технический и экономический интерес представляет процесс возгонки борной кислоты при помощи пара. Для этого пульпу из боратовой руды и серной кислоты нагревают в печах в присутствии водяного пара при 400 - 500 - при этом борная кислота возгоняется и возгон конденсируется при охлаждении в чистом виде, не требуя перекристаллизации. [9]
 |
Схема производства борной кислоты. [10] |
Выделение борной кислоты из раствора основано на различной растворимости борной кислоты и сернокислого магния при различных температурах: растворимость борной кислоты резко повышается с повышением температуры, а растворимость сернокислого магния повышается мало. [11]
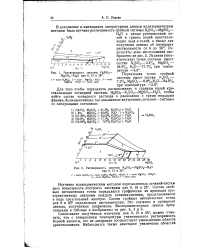 |
Растворимость системы Н3ВО3 - MgSO4 - H O при 0, 15 и 25.| Растворимость системы K2SO4 - MgSO4 - Н2О при 0, 15 и 25. [12] |
Сопоставляя полученные изотермы для 0, 15 и 25, можно отметить, что с повышением температуры увеличивается растворимость борной кислоты, что на диаграмме соответствует уменьшению области кристаллизации. [13]
Снижение концентрации сульфата магния увеличивает растворимость борной кислоты и содержание ее в маточнике, а повышение концентрации MgSO4 снижает растворимость борной кислоты. Очистку борной кислоты производят перекристаллизацией из воды при 85 - 90J в присутствии активированного угля. Технический и экономический интерес представляет процесс возгонки борной кислоты при помощи пара. Для этого пульпу из боратовой руды и серной кислоты нагревают в печах в присутствии водяного пара при 400 - 500 - при этом борная кислота возгоняется и возгон конденсируется при охлаждении в чистом виде, не требуя перекристаллизации. [14]
Были предложены также различные способы извлечения из маточных растворов товарной борной кислоты и сульфата магния, например раздельное получение борной кислоты и сульфата магния, основанное на повышении растворимости борной кислоты при введении в раствор некоторого количества окиси магния. Проверка этого способа, названного биборацией, в производственных условиях, проведенная совместно с Научно-исследовательским институтом химической промышленности Министерства местной и топливной промышленности РСФСР, показала его неэкономичность. [15]
Страницы: 1 2